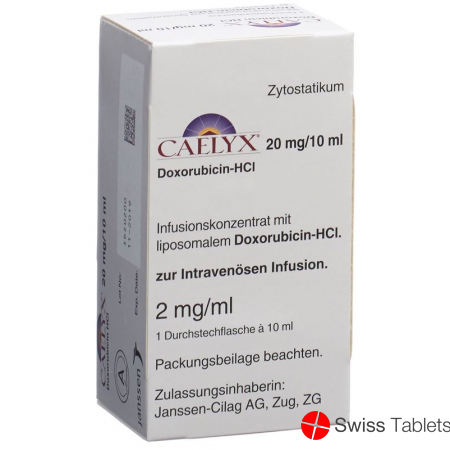
Caelyx Infusionskonzentrat 20mg/10ml Ampullen 10ml buy online
CAELYX Inf Konz 20 mg/10ml
- Availability: Not available
- Product Code: 2049855
- ATC-code L01DB01
- EAN 7680542730103
Ingredients:
Cholesterol, Natriumhydroxid, Saccharose, Histidin, Salzsäure, konzentriert, Natrium 0.54 mg, Phosphatidylcholin (Sojabohne), hydriert, MPEG 2000 Carbamoyl DSPE Natrium, Ammoniumsulfat, Doxorubicin hydrochlorid, PEG-liposomal 20 mg .
Doxorubicin hydrochlorid, PEG-liposomal 20 mg
Immunsuppressiva unterdrücken die Immunantwort beim Kontakt mit Krankheitserregern. Die Dissemination von Impfkeimen wird dadurch begünstigt und die Serokonversion beeinträchtigt. Auch abgeschwächte Keime können eine manifeste Infektion hervorrufen. Einzelne Infektionen durch Lebend-Impfstoffe unter Immunsuppressiva wurden berichtet.
Dissemination des Impfkeims und beeinträchtigte Immunantwort möglich
Immunsupprimierte Patienten, die mit Lebend-Impfstoffen geimpft werden, können in Einzelfällen eine Impfkeim-Infektion entwickeln, teils lebensbedrohlich. Ausserdem kann die Serokonversion beeinträchtigt werden.
Die Verabreichung von Lebend-Impstoffen unter immusuppressiver Behandlung ist kontraindiziert. Immunsupprimierte Patienten sollen grundsätzlich einen möglichst umfassenden Impfschutz erhalten; sie sollen die nötigen Impfungen möglichst bis 4 Wochen vor Beginn der immunsuppressiven Therapie erhalten. Die Immunantwort kann mehrere Monate nach dem Absetzen der Immunsuppressiva unterdrückt sein. Es wird meistens empfohlen, Lebend-Impfstoffe frühestens 3 Monate nach der immunsuppressiven Therapie zu verabreichen.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Natalizumab, Ocrelizumab - Immunsuppressiva und ImmunmodulatorenAdditive immunsuppressive Effekte. Das Risiko, unter der Therapie mit Natalizumab eine PML zu erleiden, lag in einer schwedischen Untersuchung von etwa 100 000 Patienten in der Grössenordnung von 1 bis 5 Promille und stieg mit der Dauer der Behandlung. Bei Vorbehandlung mit Immunsuppressiva wie Azathioprin, Mitoxantron oder Methotrexat war das Risiko zwei- bis dreimal höher.
Schwere, anhaltende Immunsuppression möglich
Bei Patienten, die vor oder während der Behandlung mit Natalizumab bzw. Ocrelizumab Immunsuppressiva oder Immunmodulatoren erhalten, kann eine starke, anhaltende Immunsuppression auftreten, die mit einem erhöhten Risiko für Infektionen, auch für opportunistische, teils lebensbedrohliche Infektionen verbunden ist. Eine progressive multifokale Leukenzephalopathie (PML), eine Virusinfektion des ZNS, kann sich entwickeln. Eine PML führt in der Regel zu schwerer Behinderung oder zum Tod. Bei gleichzeitiger Langzeit-Therapie mit hochdosierten systemischen Glukokortikoiden ist das Risiko für schwere Infektionen erhöht.
Die gleichzeitige Behandlung mit Immunsuppressiva ist kontraindiziert. Bei Patienten, die zuvor mit Immunsuppressiva bzw. Immunmodulatoren behandelt wurden, soll vor der Behandlung mit Natalizumab bzw. Ocrelizumab sicher gestellt sein, dass sie nicht mehr immungeschwächt sind. Nach dem Absetzen von Natalizumab bleiben immunsuppressive Wirkungen noch ca. 12 Wochen bestehen. Nach dem Absetzen von Ocrelizumab bleiben immunsuppressive Wirkungen im Median 72 Wochen bestehen. Glukokortikoide Eine Kurzzeit-Therapie mit systemischen Glukokortikoiden während der Behandlung mit Natalizumab bzw. Ocrelizumab ist möglich. Als Vorbehandlung gegen infusionsbedingte Reaktionen von Ocrelizumab wird Methylprednisolon empfohlen. Man geht in der Regel davon aus, dass Prednison-Dosen >=20 mg/Tag (<=10 kg: >=2 mg/kg/Tag) oder ihr Äquivalent während mindestens 2 Wochen immunsuppressiv wirken. Lokale und inhalative Glukokortikoide wirken in der Regel nicht immunsuppressiv.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Brivudin - ImmunsuppressivaDie Wirksamkeit von Brivudin in der Dosierung von 125 mg einmal täglich über 7 Tage wurde nur bei immunkompetenten Patienten untersucht. Für die Wirksamkeit bei immunsupprimierten Patienten gibt es keine klinischen Belege.
Möglicherweise verminderte Wirksamkeit von Brivudin
Bei Patienten unter immunsuppressiver Therapie ist die Wirksamkeit von Brivudin gegen Herpes zoster unsicher. Ausserdem sind Patienten mit Immunschwäche durch eine Infektion mit Herpes zoster besonders gefährdet.
Eine Infektion mit Herpes zoster bei immungeschwächten Patienten soll nicht mit Brivudin behandelt werden. Da diese Patienten durch eine Herpes-zoster-Infektion besonders gefährdet sind, sollen sie umgehend ein Virustatikum erhalten, dessen Wirksamkeit auch bei immungeschwächten Patienten belegt ist, z. B. Aciclovir.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Saccharomyces cerevisiae (boulardii) - ImmunsuppressivaImmunsuppressiva unterdrücken die Immunreaktion beim Kontakt mit Krankheitserregern. Saccharomyces-Infektionen werden dadurch begünstigt. Saccharomyces ist ein lebender Mikroorganismus, der bei immundeprimierten Patienten durch Migration aus dem Magen-Darm-Trakt in den Blutkreislauf oder durch äussere Verunreinigung von Zentralvenenkathetern generalisierte Hefeinfektionen hervorrufen kann.
Risiko für Fungämien und generalisierte Hefeinfektionen
Die gleichzeitige Behandlung mit Hefepräparaten (Saccharomyces cerevisiae bzw. boulardii) führte in Einzelfällen bei Patienten unter Immunsuppressiva zu Fungämien und Hefeinfektionen innerer Organe.
Die gleichzeitige Behandlung mit Hefepräparaten (Saccharomyces cerevisiae bzw. boulardii) ist bei Patienten unter Immunsuppressiva kontraindiziert.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Clozapin - ZytostatikaVon einer additiven Wirkung auf das Knochenmark ist auszugehen. Eine retrospektive Studie in Finnland zeigte, dass ca. 40 % aller Patienten, die unter Clozapin eine Agranulozytose entwickelten, weitere Arzneistoffe erhielten, die Agranulozytosen auslösen können. Stoffe mit dieser Nebenwirkung sind nur schwer zu benennen, da meist nur Fallberichte vorliegen. Es handelt sich um sehr viele Stoffe aus sehr unterschiedlichen Stoffgruppen.
Erhöhung des Risikos und/oder der Schwere von Granulozytopenien/Agranulozytosen
Bei gleichzeitiger Behandlung mit Clozapin und weiteren myelosuppressiven Arzneistoffen, die Agranulozytosen hervorrufen können, ist eine erhöhte Inzidenz und Schwere von Granulozytopenien und Agranulozytosen zu befürchten. Eine Agranulozytose tritt meist zu Beginn der Behandlung mit Clozapin auf, kann aber auch zu jedem späteren Zeitpunkt ausgelöst werden (siehe Kommentar).
Den Produktinformationen von Clozapin zufolge darf dieses nicht gleichzeitig mit anderen Stoffen angewandt werden, die Agranulozytosen induzieren können (Kontraindikation). Agranulozytosen sind eine schwere, aber seltene Nebenwirkung vieler lebenswichtiger Arzneistoffe. Daher können Fälle eintreten, in denen die gleichzeitige Behandlung mit Clozapin und einem dieser Arzneistoffe unumgänglich wird. In einem solchen Fall muss das Blutbild besonders engmaschig überwacht werden.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Cladribin - Immunsuppressiva und ImmunmodulatorenAdditive immunsuppressive Effekte.
Schwere, anhaltende Immunsuppression möglich
Bei Patienten, die vor oder während der Behandlung mit Cladribin Immunsuppressiva oder Immunmodulatoren (Interferon) erhalten, kann eine schwerwiegende hämatologische Toxizität bzw. eine starke, anhaltende Immunsuppression auftreten, die mit einem erhöhten Risiko für Infektionen, auch für opportunistische, teils lebensbedrohliche Infektionen verbunden ist. Bei gleichzeitiger Langzeit-Therapie mit hochdosierten systemischen Glukokortikoiden ist das Risiko für schwere Infektionen erhöht.
Die gleichzeitige Behandlung mit Immunsuppressiva ist kontraindiziert. Bei Patienten, die zuvor mit Immunsuppressiva bzw. Immunmodulatoren behandelt wurden, soll vor der Behandlung mit Cladribin sicher gestellt sein, dass sie nicht mehr immungeschwächt sind. Glukokortikoide Eine akute Kurzzeit-Therapie mit systemischen Glukokortikoiden während der Behandlung mit Cladribin ist möglich. Man geht meistens davon aus, dass Prednison-Dosen >=20 mg/Tag (<=10 kg: >=2 mg/kg/Tag) während mindestens 2 Wochen oder ihr Äquivalent immunsuppressiv sind. Lokale und inhalative Glukokortikoide wirken in der Regel nicht immunsuppressiv.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Varizellen-Lebend-Impfstoff - ImmunsuppressivaImmunsuppressiva unterdrücken die Immunantowort beim Kontakt mit Krankheitserregern. Die Dissemination von Impfkeimen wird dadurch begünstigt und die Serokonversion beeinträchtigt. Auch abgeschwächte Keime können eine manifeste Infektion hervorrufen. Einzelne Infektionen durch Lebend-Impfstoffe unter Immunsuppressiva wurden berichtet.
Dissemination des Impfkeims und beeinträchtigte Immunantwort möglich
Immunsupprimierte Patienten, die mit Lebend-Impfstoffen geimpft werden, können in Einzelfällen eine Impfkeim-Infektion entwickeln, teils lebensbedrohlich. Ausserdem kann die Serokonversion beeinträchtigt werden.
Die Verabreichung von Lebend-Impstoffen unter immusuppressiver Behandlung ist kontraindiziert. Immunsupprimierte Patienten sollen grundsätzlich einen möglichst umfassenden Impfschutz erhalten; sie sollen die nötigen Impfungen möglichst bis 4 Wochen vor Beginn der immunsuppressiven Therapie erhalten. Die Immunantwort kann mehrere Monate nach dem Absetzen der Immunsuppressiva unterdrückt sein. Es wird meistens empfohlen, Lebend-Impfstoffe frühestens 3 Monate nach der immunsuppressiven Therapie zu verabreichen. Als Alternative können hier Immunglobuline verabreicht werden.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
BCG bei Blasenkarzinom - ImmunsuppressivaDie Immunsuppressiva unterdrücken die Immunantwort beim Kontakt mit BCG, was eventuell eine Dissemination von BCG begünstigen könnte. Man geht davon aus, dass das BCG eine lokale entzündliche Reaktion, die von verschiedenen Zellen des Immunsystems, wie Makrophagen, Natural-Killer-Zellen und T-Zellen ausgelöst wird, verursacht. Immunsuppressiva können daher diese Reaktion unterdrücken.
Dissemination des Impfkeims und beeinträchtigte Therapieantwort möglich
Immunsupprimierte Patienten, die eine Instillation von lebenden abgeschwächten Mycobakterien erhalten, könnten eine BCG-Infektion entwickeln. Ausserdem könnte die Antwort auf die Therapie vermindert sein.
Die BCG-Therapie des Blasenkarzinoms darf nicht während einer immunsuppressiver Behandlung vorgenommen werden. Die gleichen Empfehlungen wie bei Lebend-Impfstoffen könnten hier auch erwogen werden: Instillation bis 4 Wochen vor Beginn der immunsuppressiven Therapie und frühestens 3 Monate nach der immunsuppressiven Therapie.
Schwerwiegende Folgen wahrscheinlich - kontraindiziert
Allergenextrakte - ImmunsuppressivaDie Wirksamkeit der spezifischen Immuntherapie setzt vermutlich ein funktionierendes Immunsystem voraus. Untersuchungen zum Einfluss einer immunsuppressiven Therapie auf die Effektivität einer Hyposensibilisierung liegen aber nicht vor.
Verminderte Wirksamkeit der Hyposensibilisierung möglich
Es wird erwartet, dass die Wirksamkeit der spezifischen Immuntherapie durch die Behandlung mit Immunsuppressiva beeinträchtigt wird.
Solange eine Immunsuppression durch immunsuppressiv wirkende Arzneimittel anhält, soll keine Hyposensibilisierung begonnen werden.
Nicht empfohlen (vorsichtshalber kontraindiziert)
Phenytoin - ZytostatikaDer Interaktion scheint ein pharmakokinetischer Mechanismus zugrunde zu liegen, da verminderte, subtherapeutische Phenytoin-Plasmakonzentrationen wurden gemessen; vermutlich spielt eine verminderte Absorption von Phenytoin auf Grund einer durch die Zytostatika geschädigten Darmschleimhaut eine Rolle. In einigen Fällen waren die Phenytoin-Plasmakonzentrationen allerdings auch vermindert, wenn Phenytoin intravenös gegeben wurde, so dass ein beschleunigter Metabolismus angenommen wurde. In einer Studie mit Patienten, die mindestens drei Zyklen Chemotherapie erhalten haben, musste die Phenytion-Dosis im Schnitt um 41 % erhöht werden. In einer zweiten Studie musste die Dosis von Phenytoin um 50 % bis 300 % erhöht werden.
Verminderte Wirksamkeit von Phenytoin/vermehrt bzw. verstärkt Blutbildschäden
In einigen Fällen traten nach 2-3 Tagen gleichzeitiger Behandlung mit Phenytoin und einigen Zytostatika (Bleomycin, Carboplatin, Carmustin, Cisplatin, Dexrazoxan, Doxorubicin, Mercaptopurin, Thiotepa, Trabectedin) verminderte Phenytoin-Plasmakonzentrationen auf, verbunden mit erhöhter Anfallshäufigkeit. Ausserdem besteht die Möglichkeit einer verstärkten Störung der Hämatopoese.
Bei gleichzeitiger Behandlung mit Phenytoin und den genannten Zytostatika soll an eine möglicherweise verminderte antikonvulsive Wirksamkeit gedacht und anhand der Plasmakonzentrationen die Phenytoin-Dosis erhöht werden. Ausserdem soll das Blutbild besonders sorgfältig kontrolliert werden.
Überwachung bzw. Anpassung nötig
Nicht-Lebendimpfstoffe - ImmunsuppressivaDie Serokonversion kann durch eine immunsuppressive Therapie beeinträchtigt werden. Die Studienlage ist sehr diskrepant. Studien zur Gabe von Influenza-Impfstoffen bei Patienten, die nach einer Organtransplantation mit Immunsuppressiva behandelt werden, zeigten entweder eine effektive Immunantwort (Azathioprin) oder deutlich verringerte Antikörperspiegel (Ciclosporin). Methotrexat verringerte die Immunantwort auf eine Pneumokokken-Impfung signifikant, während die Antikörper-Spiegel auch in Patienten unter TNFalpha-Blockern verringert waren, jedoch nicht signifikant. Die Immunantwort auf eine Influenza-Impfung wurde weder durch Methotrexat noch durch TNFalpha-Blocker verändert.
Mangelhafter Impfschutz möglich
Die Immunantwort auf Impfungen mit Nicht-Lebendimpfstoffen kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Auf Grund des erhöhten Infektionsrisikos ist eine Immunisierung von immunsupprimierten Patienten häufig indiziert (z.B. Grippe-, Pneumokokken-, Hepatitis-Impfung). Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde. Die Immunantwort kann aber in Abhängigkeit von der Intensität der Immunsuppression noch bis zu einem Jahr nach Absetzen unterdrückt sein.
Überwachung bzw. Anpassung nötig
Anthrazykline - P-Glykoprotein-InhibitorenCiclosporin hemmt das Transportprotein P-Glycoprotein, das den Transport von vielen Arzneistoffen, darunter die Anthrazykline, in das Darmlumen, die renalen Tubuli und in das Blut vermittelt. Die vermehrte Bildung von P-Glycoprotein ist eine Ursache der Zytostatika-Resistenz. Bei gleichzeitiger Anwendung mit hohen Ciclosporin-Dosen war die Bioverfügbarkeit von Doxorubicin um etwa 50 %, die seines aktiven Metaboliten Doxorubicinol um etwa 440 % erhöht. Die Hemmung von P-Glycoprotein in den Endothelzellen der Blut-Hirn-Schranke könnte die Doxorubicin-Konzentration im ZNS erhöhen und dadurch ZNS-Effekte hervorrufen, die sonst nicht auftreten.
Verstärkte Toxizität der Anthrazykline möglich
In mehreren Studien, in denen Ciclosporin in hoher Dosierung zur Überwindung einer Zytostatika-Resistenz zusammen mit Doxorubicin gegeben wurde, zeigte sich eine verstärkte Myelosuppression. Auch eine verstärkte Neurotoxizität ist nicht auszuschliessen.
Ist die gleichzeitige Anwendung mit P-Glycoprotein-Inhibitoren (Ciclosporin, Verapamil) erforderlich, sollen die Patienten sehr sorgfältig auf Anzeichen einer verstärkten Toxizität der Anthrazykline überwacht werden; bei Bedarf ist die Dosis zu senken.
Überwachung bzw. Anpassung nötig
Doxorubicin - CYP3A-InduktorenDoxorubicin ist Substrat von CYP3A4 und P-Glycoprotein, so dass die gleichzeitige Behandlung mit entsprechenden Induktoren die Clearance von Doxorubicin beschleunigt. Bei Patienten, die gleichzeitig Barbiturate erhielten, war die Clearance von Doxorubicin um 50 % höher als bei Patienten, die keine Barbiturate erhielten (318 ml/min vs. 202 ml/min).
Verminderte zytotoxische Wirksamkeit möglich
Die gleichzeitige Behandlung mit CYP3A4-Induktoren (Carbamazepin, Enzalutamid, Mitotan, Phenobarbital, Phenytoin, Primidon, Rifampicin) kann die zytotoxische Wirksamkeit von Doxorubicin beeinträchtigen.
Patienten, die mit Doxorubicin behandelt werden, sollen möglichst keine Arzneimittel erhalten, die CYP3A4 induzieren.
Überwachung bzw. Anpassung nötig
Trastuzumab - AnthrazyklineEs liegen additive kardiotoxische Effekte vor. In einer klinischen Studie wurden keine zusätzlichen pharmakokinetischen Effekte gefunden.
Risiko einer kardialen Dysfunktion/Herzinsuffizienz
Bei Patienten, die Trastuzumab erhalten, steht das Risiko einer kardialen Dysfunktion in Zusammenhang mit höheren kumulativen Anthrazyklin-Dosen, die vor der Einleitung der Behandlung mit Trastuzumab gegeben werden. Die Inzidenz einer kardialen Dysfunktion bei Behandlung mit Trastuzumab und Doxorubicin, kumulative Dosis 180 mg/m2, lag bei 1,7 %, mit Epirubicin, kumulative Dosis 300 mg/m2, bei 0,3 %.
Wenn möglich sollte eine Anthrazyklin-Therapie noch bis zu 7 Monate nach Absetzen von Trastuzumab vermieden werden. Wenn Anthrazykline eingesetzt werden, sollte die Herzfunktion des Patienten sorgfältig überwacht werden. Bei HER2-positivem Brustkrebs im Frühstadium sollen maximal kumulative Doxorubicin-Dosen von 180 mg/m2 oder Epirubicin-Dosen von 360 mg/m2 eingesetzt werden. Für andere Anthrazykline oder Indikationen sollen die aktuellen Angaben der Hersteller berücksichtigt werden.
Überwachung bzw. Anpassung nötig
Vorinostat - QT-verlängernde SubstanzenDie proarrhythmischen Wirkungen der betroffenen Substanzen könnten sich addieren oder potenzieren.
Erhöhtes Risiko für Arrhythmien (Torsade de pointes)
Bei gleichzeitiger Behandlung mit Vorinostat und QT-verlängernden Substanzen kann sich das Risiko einer proarrythmischen Wirkung inkl. Torsade de pointes erhöhen. Torsade de pointes können mit Schwindel oder Ohnmachtsanfällen einhergehen. Meist enden Torsade de pointes spontan; selten können sie in Kammerflimmern und Herzstillstand mit potenziell letalem Ausgang übergehen.
Bei gleichzeitiger Behandlung mit Vorinostat und weiteren QT-verlängernden Substanzen ist Vorsicht geboten. Elektrolytstörungen sollen vor der Anwendung korrigiert werden und das EKG überwacht werden. Bei einer Verlängerung der frequenzkorrigierten QTc-Zeit >50–60 ms bzw. >460–500 ms (unterschiedliche Grenzwerte in der Literatur angegeben) sollen die gefährdenden Arzneimittel abgesetzt werden. Ausserdem sollen die Patienten über das Risiko der Herzrhythmusstörungen informiert werden und bei Schwindel und Ohnmachtsanfällen sowie bei Durchfall oder Erbrechen (Elektrolytstörungen) umgehend einen Arzt aufsuchen.
Überwachung bzw. Anpassung nötig
CYP3A-Substrate mit enger therapeutischer Breite - CeritinibCeritinib ist ein starker CYP3A-Hemmer und kann daher die Wirkungen von CYP3A-Substraten verstärken.
Verstärkte Wirkungen der CYP3A-Substrate möglich
Bei gleichzeitiger Behandlung mit Ceritinib sind verstärkte Wirkungen von CYP3A-Substraten mit enger therapeutischer Breite nicht auszuschliessen.
Die gleichzeitige Behandlung mit Ceritinib und CYP3A-Substraten mit enger therapeutischer Breite wird im Allgemeinen nicht empfohlen; andernfalls soll die Dosierung der CYP3A-Substrate reduziert werden.
Überwachung bzw. Anpassung nötig
FSME-Impfstoffe - ImmunsuppressivaDie Serokonversion kann durch eine immunsuppressive Therapie beeinträchtigt werden. In einer Studie wiesen nach der letzten FSME-Impfung, die 1 Jahr nach der ersten Dosis verabreicht wurde, nur 39% der Patienten im Vergleich zu 79% der gesunden Probanden schützende Antikörper-Titer auf.
Mangelhafter Impfschutz möglich
Die Immunantwort auf FSME-Impfungen kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde. Die Immunantwort kann aber in Abhängigkeit von der Intensität der Immunsuppression noch bis zu einem Jahr nach Absetzen unterdrückt sein. Der Antikörper-Titer sollte 4 Wochen nach der 2. Impfung bestimmt und, falls zu diesem Zeitpunkt keine Serokonversion stattgefunden hat, eine zusätzliche Impfdosis verabreicht werden. Die 3. Impfung soll dann im vorgesehehnen zeitlichen Abstand erfolgen.
Überwachung bzw. Anpassung nötig
FSME-Impfstoffe - ImmunsuppressivaDie Serokonversion kann durch eine immunsuppressive Therapie beeinträchtigt werden. In einer Studie wiesen nach der letzten FSME-Impfung, die 1 Jahr nach der ersten Dosis verabreicht wurde, nur 39% der Patienten im Vergleich zu 79% der gesunden Probanden schützende Antikörper-Titer auf.
Mangelhafter Impfschutz möglich
Die Immunantwort auf FSME-Impfungen kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde. Die Immunantwort kann aber in Abhängigkeit von der Intensität der Immunsuppression noch bis zu einem Jahr nach Absetzen unterdrückt sein. Der Antikörper-Titer sollte 30–60 Tage nach der 2. Impfung (konventionnelles Schema) bzw. nach der 3. Impfung (Schnellschema) bestimmt und gegebenenfalls eine zusätzliche Impfdosis verabreicht werden.
Überwachung bzw. Anpassung nötig
Hepatitis-A oder -B-Impfstoffe - ImmunsuppressivaDie Serokonversion kann durch eine immunsuppressive Therapie beeinträchtigt werden. In einer Studie nach Lebertransplantation entwickelten 66% der Patienten, die eine Triple-Therapie (Ciclosporin, Steroide, Azathioprin), 84% Patienten mit einer Doppel-Therapie (Ciclosporin, Steroide) und 100% Patienten mit einer Ciclosporin-Monotherapie eine positive Immunantwort auf eine Hepatitis-B-Impfung.
Mangelhafter Impfschutz möglich
Die Immunantwort auf Hepatitis-Impfungen kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Auf Grund des erhöhten Infektionsrisiko ist eine Immunisierung von immunsupprimierten Patienten häufig indiziert. Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde. Die Immunantwort kann aber in Abhängigkeit von der Intensität der Immunsuppression noch bis zu einem Jahr nach Absetzen unterdrückt sein. Unter Umständen werden mit der Grundimmunisierung keine adäquaten Antikörper-Titer erreicht, zustäztliche Impfdosen können erforderlich sein.
Überwachung bzw. Anpassung nötig
Herpes-Zoster-Impfstoff (rekombinant, adjuvantiert) - ImmunsuppressivaDie Serokonversion kann durch eine immunsuppressive Therapie beeinträchtigt werden. Studien bei immunsupprimierten Patienten haben im Monat 13 eine positive Impfantwort bei ca. 40–50% der Patienten mit Stammzelltransplantation, soliden Tumoren oder malignen hämatologischen Krankheiten und bei 67% der Nierentransplantierten gezeigt.
Mangelhafter Impfschutz möglich
Die Immunantwort auf Herpes-Zoster-Impfstoff kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Auf Grund des erhöhten Infektionsrisiko ist eine Immunisierung von immunsupprimierten Patienten häufig indiziert. Patienten können eventuell von einem kürzeren Impfschema profitieren, in diesem Fall kann die 2. Dosis 1–2 Monate nach der ersten verabreicht werden. Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde. Die Immunantwort kann aber in Abhängigkeit von der Intensität der Immunsuppression noch bis zu einem Jahr nach Absetzen unterdrückt sein.
Überwachung bzw. Anpassung nötig
COVID-19-mRNA-Impfstoffe - ImmunsuppressivaDie Serokonversion wird durch eine immunsuppressive Therapie beeinträchtigt. In mehreren Studien wurde bestätigt, dass immunsupprimierte Patienten tiefere Antikörperspiegel aufweisen. Eine Studie hat jedoch gezeigt, dass eine dritte Dosis 28 Tage nach der zweiten Dosis einen signifikanten Anstieg neutralisierender Antikörper auszulösen vermochte. Inwieweit dies einen Schutz vor schweren Formen von COVID-19 verleiht, ist derzeit nicht bekannt.
Mangelhafter Impfschutz möglich
Die Immunantwort auf COVID-Impfungen kann durch eine immunsuppressive Therapie beeinträchtigt werden; u.a. können die erreichten Antikörper-Titer ungenügend sein.
Bei immunsupprimierten Patienten wird eine dritte Dosis 28 Tage nach der zweiten Dosis empfohlen. Auf Grund des erhöhten Infektionsrisikos ist eine Immunisierung von immunsupprimierten Patienten häufig indiziert. Wenn möglich, soll mit dem Beginn der Behandlung 2 Wochen nach der Impfung abgewartet werden. Patienten, die innerhalb von 14 Tagen vor Beginn einer immunsuppressiven Therapie oder während der Behandlung geimpft wurden, sollten als nicht immunisiert gelten und frühestens 3 Monate nach Ende der Therapie erneut geimpft werden, falls ihre Immunkompetenz wiederhergestellt wurde.
Überwachung bzw. Anpassung nötig
P-Glykoprotein-Substrate mit enger therapeutischer Breite - TepotinibTepotinib ist ein Hemmer des P-Glykoproteins und kann daher die Wirkungen der P-Glykoprotein-Substrate verstärken. Wiederholte Gabe von Tepotinib (450 mg einmal täglich) erhöhte die AUC von Dabigatranetexilat auf das 1.5-Fache und dessen Cmax auf das 1.4-Fache.
Verstärkte Wirkungen der P-Glykoprotein-Substrate möglich
Bei gleichzeitiger Behandlung mit Tepotinib sind verstärkte Wirkungen der P-Glykoprotein-Substrate mit enger therapeutischer Breite möglich.
Laut Fachinformation von Tepotinib wird die gleichzeitige Behandlung mit P-Glykoprotein-Substraten mit enger therapeutischer Breite im Allgemeinen nicht empfohlen; andernfalls soll die Fachinformation des jeweiligen P-Glykoprotein-Substrates konsultiert werden und deren Empfehlungen beachtet werden.
Überwachung bzw. Anpassung nötig
CYP3A-Substrate mit enger therapeutischer Breite - IdebenonIdebenon ist ein schwacher CYP3A-Inhibitor und kann den Metabolismus von CYP3A-Substraten mit enger therapeutischer Breite hemmen.
Verstärkte Wirkungen der CYP3A-Substrate möglich
Die gleichzeitige Behandlung mit Idebenon kann möglicherweise die Wirkungen von CYP3A-Substraten mit enger therapeutischer Breite verstärken.
Bei gleichzeitiger Behandlung mit Idebenon wird eine sorgfältige Überwachung auf verstärkte Wirkungen der genannten CYP3A-Substrate bzw. von deren Plasmakonzentrationen empfohlen.
Vorsichtshalber überwachen
BCRP-Substrate - Leflunomid, TeriflunomidLeflunomid und Teriflunomid sind Inhibitoren des Efflux-Transporters BCRP (Breast Cancer Resistance Protein) und können möglicherweise die Elimination von BCRP-Substraten hemmen und damit deren Wirkungen verstärken.
Verstärkte Wirkungen der BCRP-Substrate möglich
Die gleichzeitige Behandlung mit den BCRP-Inhibitoren Leflunomid bzw. Teriflunomid kann die substanzspezifischen Wirkungen von BCRP-Substraten (Daunorubicin, Doxorubicin, Sulfasalazin, Topotecan) möglicherweise verstärken.
Leflunomid bzw. Teriflunomid und die genannten BCRP-Substrate sollen mit Vorsicht gleichzeitig eingesetzt werden. Die Patienten sollen engmaschig auf Symptome einer Überdosierung der BCRP-Substrate überwacht und deren Dosierungen bei Bedarf verringert werden.
Vorsichtshalber überwachen
BCRP-Substrate - AcalabrutinibAcalabrutinib ist ein BCRP-Inhibitor und kann die Exposition gegenüber BCRP-Substraten erhöhen. Die Interaktion wurde nicht untersucht.
Verstärkte Wirkung von BCRP-Substraten möglich
Bei gleichzeitiger Behandlung mit BCRP-Substraten und Acalabrutinib wird eine verstärkte Wirkung der BCRP-Substrate erwartet.
Bei gleichzeitiger Behandlung mit BCRP-Substraten und Acalabrutinib ist Vorsicht geboten; Patienten sollen auf UAW der genannten Substrate überwacht werden.Oral verabreichte BCRP-Substrate mit geringer therapeutischer Breite sollten mindestens 6 h vor oder nach Acalabrutinib eingenommen werden.
Vorsichtshalber überwachen
BCRP-Substrate - TepotinibTepotinib ist ein BCRP-Inhibitor und kann die Exposition gegenüber BCRP-Substraten erhöhen.
Verstärkte Wirkung von BCRP-Substraten möglich
Bei gleichzeitiger Behandlung mit BCRP-Substraten und Tepotinib wird eine verstärkte Wirkung der BCRP-Substrate erwartet.
Bei gleichzeitiger Behandlung mit BCRP-Substraten und Tepotinib ist Vorsicht geboten; Patienten sollen auf UAW der genannten Substrate überwacht werden.
Vorsichtshalber überwachen

Description
Caelyx 20 mg/10 ml Solution is a pharmaceutical product presented as a 10 ml solution, designed for intravenous administration. It contains 20 mg of the active ingredient per 10 ml, formulated to ensure precise dosing and effective delivery. This solution is typically used under medical supervision as part of a treatment regimen.
The product is supplied in a ready-to-use liquid form, facilitating ease of preparation and administration in clinical settings. Its formulation is intended to maintain stability and potency, ensuring consistent therapeutic performance.
Key features of Caelyx 20 mg/10 ml Solution include:
- Pre-measured 10 ml solution for accurate dosing
- Contains 20 mg of active substance per vial
- Sterile and suitable for intravenous use
- Formulated for stability and ease of administration
- Used under professional healthcare guidance
This product is intended for use in specific medical treatments as prescribed by healthcare professionals. Proper handling and administration are essential to ensure safety and effectiveness. Always follow the instructions provided by your healthcare provider when using Caelyx 20 mg/10 ml Solution.
Reviews (0)
Write a review
Recently Viewed
Clexane 100 mg/ml 10 prefilled syringes 1 ml solution
Was ist Clexane und wann wird es angewendet? Nach operativen Eingriffen oder bei Bettlägerigkeit bes..
180.18 CHF
Bisolvon Phyto 120 ml sugar-free cough syrup
Was ist Bisolvon Phyto Complete Zuckerfrei und wann wird es angewendet?Bisolvon Phyto Complete Zucke..
30.89 CHF
Imatinib Mylan Filmtabletten 400mg 30 Stück
Was ist Imatinib Mylan und wann wird es angewendet?Imatinib Mylan enthält den Wirkstoff Imatinib, de..
1,141.67 CHF

Free consultation with an experienced pharmacist
Describe the symptoms or the right drug - we will help you choose its dosage or analogue, place an order with home delivery or just consult.
We are 14 pharmacists and 0 bots. We will always be in touch with you and will be able to communicate at any time.
Bestsellers
Milupa Aptamil Pepti Syneo 400 g powder
Product code: 7748334Aptamil Pepti Syneo is a special food for babies from birth who are allergic to cow's milk protein a..
55.08 CHF
Weleda Baby Calendula Wind- und Wetterbalsam 30ml
Product code: 5455461Der Weleda Baby Calendula Wind- und Wetterbalsam schützt die sensible Babyhaut intensiv bei Kälte un..
15.35 CHF
HerpoTherm herpes pen
Product code: 7798882Herpotherm® - the heating pen Cold sores are not only unattractive but can also be very painful. Th..
78.48 CHF
Herba 17 cm 10 pieces cardboard nail files
Product code: 1070557Herba 17 cm 10 Pieces Cardboard Nail Files are essential grooming tools designed to help you maintai..
10.06 CHF
Atolur 40 mg 60 capsules
Product code: 7805275Atolur 40 mg 60 capsules is a pharmaceutical product designed for oral administration in capsule for..
76.22 CHF
Blistex Classic Stick 4.2 g stick
Product code: 7813615The Blistex Classic Stick 4.2 g is a convenient lip care product designed to provide effective moist..
15.03 CHF
Emoform Brush'n Clean 80 pieces
Product code: 5667499Metallfreie Interdentalbürsten. Die kleine, elastische Gummibürste passt sich optimal dem Zahnzwisch..
34.61 CHF
Flatulex 50 Kautabletten
Product code: 1647264Was ist Flatulex und wann wird es angewendet?Flatulex ist ein Arzneimittel zur Behandlung von Beschw..
17.88 CHF