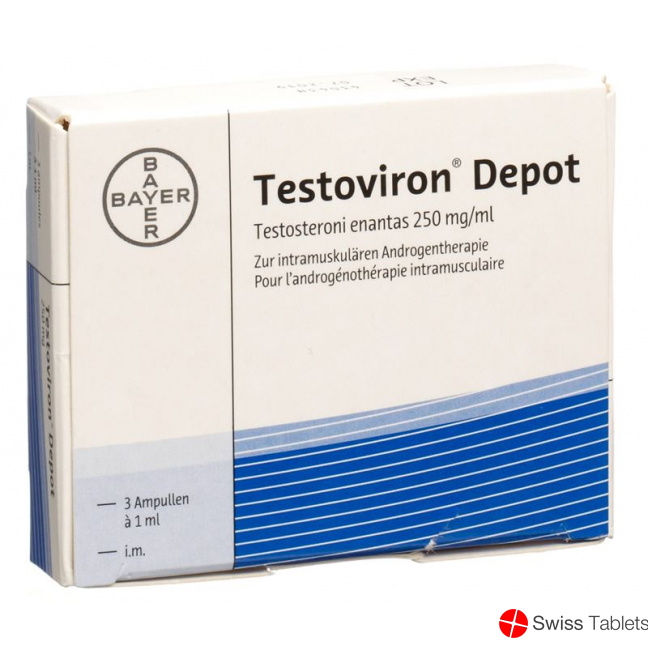
Testoviron Depot Injektionslösung 250mg i.m. Ampullen 3 Stück buy online
Testoviron Depot Inj Lös 250 mg i.m. Amp 3 Stk
-
106.21 CHF
- Price in reward points: 3131

- Availability: In stock
- Brand: BAYER PHARMACEUTICALS
- Product Code: 425509
- ATC-code G03BA03
- EAN 7680176260359
Ingredients:
Benzyl benzoat, Testosteron 178 mg, Rizinusöl, Testosteron enantat 250 mg .

Description
Testoviron Depot 250 mg 3 pieces injection solution is a pharmaceutical product designed for intramuscular injection. It contains testosterone enanthate, a synthetic form of the naturally occurring male hormone testosterone. This medication is typically used in hormone replacement therapy to address conditions associated with low testosterone levels.
The product comes in a pack of three ampoules, each containing 250 mg of the active ingredient in an oil-based solution. The injection solution is intended for deep intramuscular administration, allowing for a slow and sustained release of testosterone into the bloodstream.
Key features and benefits:
- Provides a controlled and prolonged release of testosterone.
- Supports the maintenance of normal male secondary sexual characteristics.
- Available in a convenient pack of three ampoules for multiple doses.
- Formulated as an injection solution for effective absorption.
Testoviron Depot 250 mg should be used under medical supervision, with dosage and frequency determined by a healthcare professional based on individual needs. Proper administration technique and adherence to prescribed schedules are important for optimal results.
Reviews (0)
Recently Viewed

Free consultation with an experienced pharmacist
Describe the symptoms or the right drug - we will help you choose its dosage or analogue, place an order with home delivery or just consult.
We are 14 pharmacists and 0 bots. We will always be in touch with you and will be able to communicate at any time.