Hemangiol Lös 3.75 mg / ml Fl 120 ml
Hemangiol Lös 3.75 mg/ml Fl 120 ml
-
367.85 CHF
- Price in reward points: 3131

- Availability: In stock
- Brand: PIERRE FABRE SUISSE AG
- Product Code: 6112208
- ATC-code C07AA05
- EAN 7680612140016
Ingredients:
Propranolol 3.75 mg, Hydroxyethylcellulose, Propylenglycol 2.60 mg, Natrium 0.17 mg, Saccharin natrium-2-Wasser, Propranolol hydrochlorid 4.28 mg , Citronensäure-Monohydrat, Erdbeer-Aroma, Vanille-Aroma.

Description
Was ist Hemangiol und wann wird es angewendet?
Hemangiol Lösung enthält den Wirkstoff Propranolol. Propranolol gehört zu einer als Betablocker bekannten Gruppe von Arzneimitteln. Dieses Arzneimittel wird zur Behandlung von proliferativen infantilen Hämangiomen, die eine systemische Therapie erfordern, eingesetzt.
Die Therapie wird bei Säuglingen zwischen 5 Wochen und 5 Monaten zu Beginn der Behandlung angewendet.
Ein Hämangiom ist eine Ansammlung von zusätzlichen Blutgefässen, die ein Geschwulst in oder unter der Haut gebildet haben. Ein Hämangiom kann oberflächlich oder tief sitzen. Manchmal wird es auch mit «Blutschwamm» oder «Erdbeerfleck» bezeichnet, da die Oberfläche des Hämangioms ein wenig wie eine Erdbeere aussieht.
Wann darf Hemangiol nicht eingenommen / angewendet werden?
Hemangiol darf nicht eingenommen werden, wenn das Kind:
- zu früh geboren wurde und noch nicht das korrigierte Alter von 5 Wochen erreicht hat (das korrigierte Alter ist das Alter, das das Frühgeborene haben würde, wenn es an seinem erwarteten Geburtstermin geboren wäre);
- unter 2 kg wiegt;
- allergisch ist gegen Propranolol oder gegen einen der sonstigen Inhaltsstoffe dieses Arzneimittels. Eine allergische Reaktion kann sich z.B. durch Hautausschlag, Juckreiz oder Kurzatmigkeit manifestieren;
- Asthma hat oder bereits früher einmal Atembeschwerden hatte;
- eine für sein Alter niedrige Herzfrequenz hat; bitte wenden Sie sich an Ihren Arzt, wenn Sie nicht sicher sind.
- Herzprobleme hat (wie z.B. Herzrhythmusstörungen und Herzinsuffizienz);
- einen sehr niedrigen Blutdruck hat;
- Durchblutungsstörungen hat, bei denen die Zehen und Finger taub und blass sind;
- zu einem niedrigen Blutzuckerspiegel neigt;
- einen hohen Bluthochdruck hat, der infolge eines Nebennierentumors verursacht wird. Dies wird als «Phäochromozytom» bezeichnet.
Geben Sie Ihrem Kind dieses Arzneimittel NICHT, wenn Sie Ihr Kind stillen, und wenn Sie selber Arzneimittel einnehmen, die nicht zusammen mit Hemangiol® angewendet werden dürfen (siehe Rubrik «Wenn Sie Ihr Kind stillen» und «Andere Arzneimittel und Hemangiol»).
Wann ist bei der Einnahme / Anwendung von Hemangiol Vorsicht geboten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Ihrem Kind Hemangiol® geben:
- Wenn Ihr Kind an einer Erkrankung der Leber oder Nieren leidet. Dieses Arzneimittel wird bei Leber- oder der Nierenerkrankungen nicht empfohlen.
- Wenn bei Ihrem Kind jemals eine allergische Reaktion aufgetreten ist. Eine allergische Reaktion kann ein Hautausschlag, Juckreiz oder Kurzatmigkeit sein.
- Wenn Ihr Kind unter Psoriasis leidet (eine Hauterkrankung, bei der rote, trockene Platten verdickter Haut auftreten), da dieses Arzneimittel die Symptome dieser Erkrankung verstärken kann.
- Wenn Ihr Kind an der Zuckerkrankheit (Diabetes) leidet: In diesem Fall ist die Überwachung des Blutzuckerspiegels zu intensivieren.
- Wenn Ihr Kind unter dem PHACE-Syndrom leidet (eine Erkrankung, bei der Hämangiome zusammen mit Gefässanomalien, auch der Blutgefässe im Gehirn, auftreten), da sich dadurch das Schlaganfallrisiko erhöhen kann.
Wichtige Anzeichen, die nach der Verabreichung von Hemangiol zu überwachen sind:
Hypoglykämierisiko
Dieses Arzneimittel kann Warnzeichen einer Hypoglykämie (niedriger Blutzuckerspiegel) maskieren. Es kann auch die Hypoglykämie bei Kindern verschlimmern, insbesondere während der Nüchternzeit (z.B. schlechte orale Nahrungsaufnahme, begleitende Infektionen, Erbrechen), bei erhöhtem Glukosebedarf (Kälte, Stress, Infektionen) oder im Falle einer Überdosierung. Diese Warnzeichen können sein:
- Wenig schwerwiegende Symptome: Blässe, Müdigkeit, Schwitzen, Zittern, Herzklopfen, Angstzustände, Hunger, Schwierigkeiten aufzuwachen.
- Schwerwiegende Symptome: Übermässiges Schlafen, verminderte Ansprechbarkeit, reduzierte Nahrungsaufnahme, Abfall der Körpertemperatur, Konvulsionen (Krampfanfälle), unregelmässige Atmung, Bewusstseinsverlust.
Zur Vermeidung einer Hypoglykämie, sollten Sie HEMANGIOL während oder direkt nach einer Fütterung verabreichen und vermeiden, die letzte Dosis kurz vor dem Zubettgehen zu verabreichen. Ihr Kind muss während der Behandlung ausreichend und regelmässig gefüttert werden. Wenn Ihr Kind nicht ausreichend isst, eine andere Krankheit entwickelt oder erbricht, wird empfohlen, die Dosis auszulassen. VERABREICHEN SIE IHREM KIND DIE NÄCHSTE HEMANGIOL®-GABE ERST WIEDER, NACHDEM ES AUSREICHEND NAHRUNG ZU SICH GENOMMEN HAT
Zeigt Ihr Kind während der Einnahme von Hemangiol irgendwelche Anzeichen einer Hypoglykämie, brechen Sie die Behandlung ab und rufen sofort einen Arzt an oder gehen Sie direkt ins Krankenhaus. Wenn das Kind bei Bewusstsein ist, geben Sie ihm, eine zuckerhaltige Flüssigkeit zu trinken.
Bronchospasmusrisiko
Wenn Sie nach Gabe von Hemangiol folgende Symptome beobachten, bei denen Verdacht auf einen Bronchospasmus besteht (d.h. vorübergehende Atemschwierigkeiten hervorgerufen durch Einengung der Bronchien), brechen Sie die Behandlung ab und benachrichtigen Sie unverzüglich einen Arzt. Husten, schnelles oder schweres Atmen oder Keuchen, zusammen mit oder ohne bläulich verfärbte Haut sind Hinweise für einen Bronchospasmus.
Beenden Sie die Behandlung und suchen Sie sofort einen Arzt auf, wenn Ihr Kind während der Einnahme von HEMANGIOL kälteähnliche Symptome in Verbindung mit Atembeschwerden und/oder Keuchen aufweist.
Risiko einer Hypotonie und Bradykardie (niedrige Herzfrequenz)
Hemangiol kann zu einer Blutdrucksenkung (Hypotonie) und einer Verringerung der Herzfrequenz (Bradykardie) führen. Daher wird Ihr Kind bei Beginn der Behandlung bzw. nach der ersten Einnahme und im Falle einer Dosiserhöhung für 4 Stunden unter enger ärztlicher Aufsicht klinisch überwacht und die Herzfrequenz kontrolliert. Danach wird Ihr Kind während der weiteren Behandlung regelmässig einer klinischen Untersuchung unterzogen.
Kontaktieren Sie Ihren Arzt unverzüglich, wenn Ihr Kind während der Einnahme von HemangiolAnzeichen von Müdigkeit, Kälte, Blässe, blau gefärbte Haut oder Ohnmacht zeigt. |
Hyperkaliämierisiko
Hemangiol kann den Kaliumspiegel im Blut erhöhen (Hyperkaliämie), wenn ein grosses ulzeriertes Hämangiom vorliegt. In diesem Fall sollte der Kaliumspiegel Ihres Kindes im Blut gemessen werden.
Wenn ihr Kind einer Vollnarkose unterzogen werden soll
Der Blutdruck Ihres Kindes kann abfallen, wenn ihm bei der Aufnahme dieses Arzneimittels bestimmte Narkosemittel gegeben werden. Informieren Sie den Anästhesisten bzw. die Anästhesistin, dass Ihr Kind Hemangiol einnimmt und er/sie wird entscheiden, ob und für wie lange die Behandlung mit Hemangiol vor dem chirurgischen Eingriff abgesetzt wird.
Einnahme von Hemangiolzusammen mit anderen Arzneimitteln
- Informieren Sie Ihren Arzt oder Apotheker oder Ihr medizinisches Fachpersonal, wenn Sie Ihrem Kind andere Arzneimittel geben, kürzlich andere Arzneimittel gegeben haben oder beabsichtigen, ihm andere Arzneimittel zu geben. Hemangiol® kann die Art der Wirkung anderer Arzneimittel beeinflussen sowie auch andere Arzneimittel die Wirkung von Hemangiolbeeinflussen können.
- Wenn Sie Ihr Kind stillen, ist es darüber hinaus wichtig, Ihren Arzt oder Apotheker oder Ihr medizinisches Fachpersonal zu informieren, welche Arzneimittel Sie selbst einnehmen, da diese in Ihre Muttermilch übergehen und die Behandlung Ihres Kindes beeinträchtigen können. Ihr Arzt wird Sie darüber informieren ob Sie das Stillen einstellen sollen oder nicht.
- Informieren Sie Ihren Arzt oder Apotheker wenn Ihr Kind andere Arzneimittel einnimmt, insbesondere:
- Arzneimittel gegen Diabetes
- Arzneimittel zur Behandlung von Herz- und Gefässkrankheiten, wie z.B. unregelmässiger Herzschlag, Brustschmerzen oder Angina, Bluthochdruck, Herzinsuffizienz,
- Arzneimittel zur Behandlung von Angstzuständen und Depressionen sowie schwerwiegendere psychische Erkrankungen und Epilepsie,
- Arzneimittel zur Behandlung von Tuberkulose,
- Arzneimittel zur Behandlung von Schmerzen und Entzündungen,
- Arzneimittel zur Senkung des Blutfettspiegels,
- Arzneimittel, die zur Narkose eingesetzt werden.
Bei weiteren Fragen wenden Sie sich bitte an Ihren Arzt, Apotheker bzw. Ärztin, Apothekerin.
Hemangiol enthält weniger als 1 mmol Natrium (23 mg) pro Flasche, d.h. es ist im Wesentlichen «natriumfrei».
Die maximale tägliche Dosis Hemangiol enthält 2,08 mg Propylenglykol/kg/Tag.
Wenn Ihr Baby weniger als 4 Wochen alt ist, sprechen Sie mit Ihrem Arzt oder Apotheker bevor Sie ihm dieses Arzneimittel geben, insbesondere, wenn Ihr Baby gleichzeitig andere Arzneimittel erhält, die Propylenglycol oder Alkohol enthalten.
Darf Hemangiol während einer Schwangerschaft oder in der Stillzeit eingenommen / angewendet werden?
Wenn Sie Ihr Kind stillen:
- Informieren Sie Ihren Arzt bzw. Ärztin darüber, bevor er bzw. sie Ihnen dieses Arzneimittel verschreibt.
- Verabreichen Sie Ihrem Kind dieses Arzneimittel nicht, wenn Sie ihrerseits Arzneimittel einnehmen, die nicht zusammen mit Hemangiol® angewendet werden sollten.
Wie verwenden Sie Hemangiol?
Die Behandlung wurde bei Ihrem Kind von einem Arzt eingeleitet, der über Erfahrung bei der Diagnose und in der Behandlung infantiler Hämangiome verfügt.
Geben Sie Ihrem Kind dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker. Fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie nicht sicher sind.
Ändern Sie niemals selbst die Dosis, die Sie Ihrem Kind verabreichen. Jede Erhöhung der Dosis oder jede Anpassung der Dosis an das Gewicht Ihres Babys muss durch Ihren Arzt erfolgen.
Dosierung
Die Dosierung basiert auf dem Gewicht Ihres Babys, entsprechend folgendem Schema:
Wochen | Einnahmedosis | Einnahmedosis | Zeit der Einnahme |
Erste Woche (1 mg/kg/Tag oder 0.3 ml/kg) | 0.5 mg/kg | 0.15 ml/kg |
|
Zweite Woche (2mg/kg/Tag oder 0.6 ml/kg) | 1 mg/kg | 0.3 ml/kg | |
Dritte und folgende Wochen (3 mg/kg/Tag oder 0.8 ml/kg) | 1.5 mg/kg | 0.4 ml/kg |
Wie geben Sie Ihrem Kind Hemangiol?
- Das Arzneimittel wird während oder direkt nach der Mahlzeit verabreicht
- Die Dosis muss immer mithilfe der mit der Flasche gelieferten Oralspritze abgemessen werden.
- Verabreichen Sie Hemangiol direkt in den Mund des Kindes und verwenden Sie dabei die Oralspritze die der Flasche beigelegt ist. Falls erforderlich, können Sie das Arzneimittel in einer kleinen Menge Säuglingsmilch oder altersgerecht mit Apfel- und / oder Orangensaft vermischen und Ihrem Kind in einer Babyflasche verabreichen. Vermischen Sie das Arzneimittel nicht in einer vollen Milch- oder Saftflasche.
Bei Kindern mit einem Gewicht von bis zu 5 kg können Sie die Dosis mit einem Teelöffel Milch (rund 5 ml) vermischen. Bei Kindern mit einem Gewicht von mehr als 5 kg kann die Dosis mit einem Esslöffel Milch oder Fruchtsaft (rund 15 ml) vermischt werden.
Verwenden Sie die Mischung innerhalb von 2 Stunden. - Geben Sie Ihrem Kind regelmässig zu essen, um längere Hungerperioden zu vermeiden.
- Wenn Ihr Kind nicht isst oder erbricht, wird empfohlen, die Dosis auszulassen.
- Wenn Ihr Kind eine Dosis wieder ausspuckt oder wenn Sie unsicher sind, ob es die gesamte verabreichte Dosis zu sich genommen hat, geben Sie keine weitere Dosis, warten Sie einfach bis zur nächsten geplanten Dosis.
- Hemangiol und die Nahrung müssen von derselben Person gegeben werden, um das Risiko einer Hypoglykämie (Unterzuckerung) zu vermeiden. Wenn mehrere Personen einbezogen sind, ist eine gute Kommunikation von wesentlicher Bedeutung, um die Sicherheit Ihres Kindes zu gewährleisten.
Halten Sie sich an die in der Packungsbeilage angegebene oder vom Arzt oder von der Ärztin verschriebene Dosierung. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt, Apotheker bzw. mit Ihrer Ärztin, Apothekerin.
Gebrauchsanleitung:
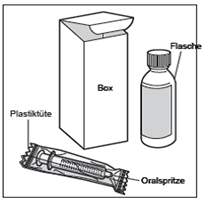
Schritt 1: Herausnehmen der Artikel aus der Box.
Die Box enthält folgende Elemente, die Sie zur Verabreichung des Arzneimittels benötigen werden:
- eine Glasflasche mit 120 ml Propranolol, Lösung zum Einnehmen.
- eine Oralspritze mit einer Skala in mg, die mit dem Arzneimittel mitgeliefert wird.
Nehmen Sie die Flasche und die Oralspritze aus der Box und entnehmen Sie die Spritze aus der Plastiktüte.
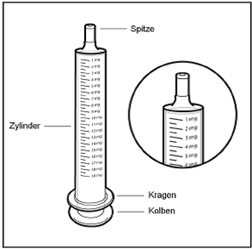
Schritt 2: Überprüfen Sie die Dosis
Überprüfen Sie die Hemangiol-Dosis in Milligramm (mg) wie vom Arzt Ihres Kindes verschrieben. Lesen Sie diese Zahl an der Skalierung der Oralspritze ab.
Schritt 3: Öffnen Sie die Flasche
Die Flasche wird mit einem Verschluss mit Kindersicherung mitgeliefert. Um die Flasche öffnen zu können, drücken Sie den Plastikverschluss nach unten, während Sie den Verschluss gegen den Uhrzeigersinn drehen (nach links).
Die Flasche vor Gebrauch nicht schütteln.
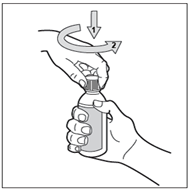
Schritt 4: Führen Sie die Spritze ein
Führen Sie die Spitze der Oralspritze in die Flasche ein, die Sie dabei aufrecht halten und drücken Sie den Kolben ganz bis nach unten.
Den Spritzenadapter nicht vom Flaschenhals entfernen.
Verwenden Sie zur Messung und Verabreichung der Dosis nur die Oralspritze, die mit dem Arzneimittel mitgeliefert wurde. Benutzen Sie keinen Löffel oder sonstige anderweitige Abgabevorrichtungen.
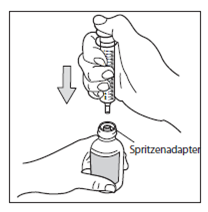
Schritt 5: Entnahme der Dosis
Drehen Sie die Flasche mit dem Kopf nach unten, wobei die Oralspritze in die Flasche steckenbleibt.
Ziehen Sie den Kolben der Spritze bis zur benötigten Dosis Milligramm heraus.
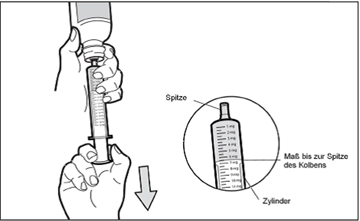
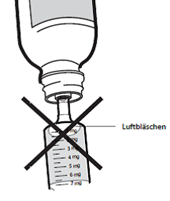
Schritt 6: Auf Luftbläschen überprüfen
Wenn Sie Luftbläschen in der Spritze sehen, halten Sie die Spritze aufrecht, schieben Sie den Kolben weit genug nach oben, um alle grossen Luftbläschen komplett auszustossen und passen Sie die von Ihrem Arzt verschriebene Dosis erneut an.
Schritt 7: Entfernen Sie die Spritze
Stellen Sie die Flasche wieder aufrecht hin und ziehen Sie die Oralspritze am Zylinder ganz aus der Flasche heraus. Beachten Sie, dass Sie dabei nicht am Kolben ziehen oder den Kolben wieder in die Spritze schieben
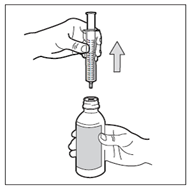
Schritt 8: Schliessen Sie die Flasche
Setzen Sie den Plastikverschluss wieder auf die Flasche auf, indem Sie diesen im Uhrzeigersinn (nach rechts) zudrehen.
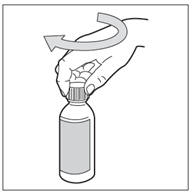
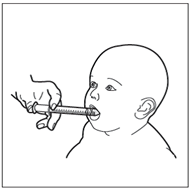
Schritt 9: Geben Sie Ihrem Kind das Hemangiol
Führen Sie die Spritze in den Mund Ihres Babys ein und legen Sie diese an der Innenseite seiner Wange an.
Jetzt können Sie Hemangiollangsam aus der Spritze direkt in den Mund Ihres Babys abgeben.
Legen Sie Ihr Kind nicht direkt nach der Verabreichung hin.
Schritt 10: Reinigen Sie die Spritze.
Zerlegen Sie die Spritze nicht. Spülen Sie die leere Spritze nach jeder Benutzung in einem Glas mit sauberem Wasser:
- Nehmen Sie ein Glas mit sauberem Wasser
- Schieben Sie den Zylinder mit Kolben hinein um die Oralspritze zu spülen
- Entsorgen Sie das Wasser in Ihrem Ausguss
- Wiederholen Sie diesen Reinigungsvorgang 3 Mal.
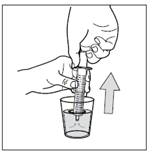
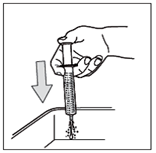
Verwenden Sie zum Reinigen kein Produkt auf Seifen- oder Alkoholbasis. Wischen Sie die Aussenseite trocken.
Reinigen Sie die Spritze nicht in einer Geschirrspülmaschine oder einem Sterilisator.
Bewahren Sie die Flasche und die Spritze bis zur nächsten Verwendung in der Kartonbox an einem sicheren Ort auf, an einem sicheren Ort ausserhalb der Sicht- und Reichweite Ihres Kindes auf. Entsorgen Sie die Spritze, sobald die Flasche aufgebraucht ist.
Wenn Sie Ihrem Kind eine grössere Menge Hemangiol gegeben haben, als Sie sollten
Wenn Sie Ihrem Kind mehr Hemangiol gegeben haben, als Sie sollten, suchen Sie bitte unverzüglich Ihren Arzt auf.
Wenn Sie die Gabe von Hemangiol für Ihr Kind vergessen haben
Geben Sie nicht die doppelte Menge, wenn Sie die vorherige Gabe vergessen haben. Setzen Sie die Behandlung erst zum nächsten vorgesehenen Zeitpunkt fort, d.h. je eine Dosis am Morgen und je eine am späten Nachmittag.
Wenn Sie die Anwendung von Hemangiol für Ihr Kind abbrechen
Hemangiol kann bei Abschluss der Behandlung, wie vom Arzt festgelegt, unverzüglich abgesetzt werden.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker bzw. an Ihre Ärztin oder Apothekerin oder das medizinische Fachpersonal.
Halten Sie sich an die in der Packungsbeilage angegebene oder vom Arzt oder von der Ärztin verschriebene Dosierung. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt, Apotheker bzw. mit Ihrer Ärztin, Apothekerin.
Welche Nebenwirkungen kann Hemangiol haben?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem Patienten auftreten müssen.
Sehr häufig (betrifft mehr als einen von 10 Anwendern)
- Bronchitis (Entzündung der Bronchien)
- Schlafstörungen (Schlaflosigkeit, schlechte Schlafqualität und Schwierigkeiten beim Aufwachen),
- Durchfall und Erbrechen
Häufig (betrifft bis zu 1 bis 10 von 100 Anwendern)
- Bronchospasmen (Schwierigkeiten beim Atmen)
- Bronchiolitis (Entzündung der kleinen Bronchien mit Schwierigkeiten beim Atmen und pfeifenden Atemgeräuschen in der Brust) in Verbindung mit Husten und Fieber,
- Verminderter Blutdruck,
- Verminderter Appetit,
- Unruhe, Alpträume, Reizbarkeit,
- Schläfrigkeit,
- Kalte Extremitäten,
- Verstopfung, Bauschmerzen,
- Erythem (Rötung der Haut),
- Windelausschlag
Gelegentlich (betrifft 1 bis 10 von 1000 Anwendern)
- Erregungsüberleitungsstörungen oder Rhythmusstörungen (langsame oder ungleichmässige Herzschläge)
- Urtikaria (allergische Reaktion der Haut), Alopezie (Haarverlust),
- Verminderter Blutzuckerspiegel,
- Verminderte Anzahl der weissen Blutkörperchen
Häufigkeit nicht bekannt
- Konvulsionen (Muskelkrämpfe) im Zusammenhang mit Hypoglykämie (anormal niedriger Blutzuckerspiegel),
- Bradykardie (anormal niedrige Herzfrequenz),
- Niedriger Blutdruck
- Starke Abnahme der Anzahl der weissen Blutkörperchen, die Infektionen bekämpfen,
- Durchblutungsstörungen, so dass die Zehen und Finger taub und blass werden,
- Erhöhter Kaliumspiegel im Blut
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Dies gilt insbesondere auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind.
Was ist ferner zu beachten?
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Hemangiol ist gut verschlossen in der Originalverpackung und für Kinder unerreichbar bei Raumtemperatur (15-25°C) und vor Licht geschützt aufzubewahren. Das Präparat darf nicht eingefroren werden.
Dauer der Haltbarkeit nach Anbruch: 2 Monate.
Die Flasche vor Gebrauch nicht schütteln.
Weitere Auskünfte erteilt Ihnen Ihr Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in Hemangiol enthalten?
1 ml Hemangiol, Lösung zum Einnehmen enthält
Wirkstoffe
3,75 mg Propranolol (Base) als 4,28 mg Propranololhydrochlorid.
Hilfsstoffe
Vanillearoma und Erdbeeraroma (enthalten Propylenglycol), Saccharin-Natrium, Hydroxyethylcellulose (aus gentechnisch veränderter Baumwolle hergestellt), Citronensäure-Monohydrat, gereinigtes Wasser.
Zulassungsnummer
61214 (Swissmedic)
Wo erhalten Sie Hemangiol? Welche Packungen sind erhältlich?
In Apotheken nur gegen ärztliche Verschreibung.
Flasche zu 120 ml
Zulassungsinhaberin
Pierre Fabre (Suisse) S.A., Allschwil
Diese Packungsbeilage wurde im September 2020 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.
Qu’est-ce que Hemangiol et quand doit-il être utilisé?
Hemangiol contient le principe actif propranolol.
Le propranolol appartient à un groupe de médicaments connus sous le nom de bêtabloquants.
Ce médicament est utilisé pour traiter les hémangiomes infantiles prolifératifs nécessitant un traitement systémique.
Hemangiol est débuté chez des enfants âgés de 5 semaines à 5 mois.
Un hémangiome est un amas de vaisseaux sanguins supplémentaires qui ont formé une masse dans ou sous la peau. L'hémangiome peut être superficiel ou profond. Il est parfois appelé «angiome fraise» car la surface de l'hémangiome ressemble un peu à une fraise.
Quand Hemangiol ne doit-il pas être pris/utilisé?
N'administrez pas Hemangiol si votre enfant:
- est né prématuré et n'a pas atteint l'âge corrigé de 5 semaines (l'âge corrigé étant l'âge qu'aurait le prématuré s'il était né à la date prévue);
- pèse moins de 2 kg;
- est allergique au propranolol ou à l'un des autres composants contenus dans ce médicament. Une réaction allergique peut inclure une éruption, des démangeaisons ou des difficultés à respirer;
- a un asthme ou un antécédent de difficultés à respirer;
- a une fréquence cardiaque lente pour son âge. Veuillez vérifier avec votre médecin si vous avez des doutes;
- a un problème au cœur (comme des troubles du rythme cardiaque ou une insuffisance cardiaque);
- a une pression artérielle très basse;
- a des problèmes de circulation qui peuvent se traduire par un engourdissement et une pâleur des orteils et des doigts;
- a tendance à avoir un faible taux de sucre dans le sang;
- a une pression artérielle élevée en raison d'une tumeur de la glande surrénale. C'est ce que l'on appelle un «phéochromocytome».
Si vous allaitez votre enfant et si vous prenez des médicaments qui ne doivent pas être utilisés avec Hemangiol (voir «Si vous allaitez votre enfant» et «Autres médicaments et Hemangiol»), n'administrez PAS Hemangiol à votre enfant.
Quelles sont les précautions à observer lors de la prise/l’utilisation d’Hemangiol?
Adressez-vous à votre médecin avant que votre enfant reçoive Hemangiol:
- si votre enfant a des problèmes au foie ou aux reins. Ce médicament ne sera pas recommandé en cas d'insuffisance hépatique ou rénale;
- si votre enfant a déjà eu une réaction allergique. Une réaction allergique peut inclure une éruption, des démangeaisons ou un essoufflement;
- si votre enfant a un psoriasis (une maladie de peau qui produit des plaques rouges et sèches de peau épaissie), car ce médicament pourrait aggraver les symptômes de cette maladie;
- si votre enfant a un diabète: dans ce cas, la glycémie (taux de sucre dans le sang) de votre enfant doit être mesurée plus fréquemment;
- si votre enfant est atteint de syndrome PHACE (une affection associant un hémangiome et des anomalies vasculaires concernant les vaisseaux sanguins cérébraux), car ce médicament pourrait majorer le risque d'infarctus cérébral.
Signes importants à surveiller après l'administration d'Hemangiol
Risque d'hypoglycémie
Ce médicament peut masquer les signes annonciateurs d'une hypoglycémie (ou faible taux de sucre dans le sang). Il peut également aggraver les hypoglycémies survenant chez l'enfant, en particulier lors de périodes de jeûne (p.ex. difficultés à s'alimenter par voie orale, infections, vomissements), en cas de besoins accrus en glucose (froid, stress, infections) ou en cas de surdosage. Ces signes peuvent être les suivants:
- Mineurs: pâleur, fatigue, sueurs, tremblement, palpitations, anxiété, faim, difficulté à se réveiller.
- Majeurs: sommeil excessif, difficulté à répondre, diminution de la prise alimentaire, baisse de la température, convulsions (crises convulsives), respiration irrégulière, perte de connaissance.
Pour éviter les risques d'hypoglycémie, vous devez administrer HEMANGIOL pendant un repas ou directement après avoir nourri votre enfant et éviter d'administrer la dernière dose peu de temps avant le coucher. Votre enfant doit être suffisamment et régulièrement nourri pendant le traitement. Si votre enfant ne mange pas suffisamment, s'il développe une autre maladie ou s'il vomit, il est recommandé de ne pas administrer la dose. NE PAS ADMINISTRER HEMANGIOL À VOTRE ENFANT TANT QU'IL NE S'ALIMENTE PAS DE NOUVEAU CORRECTEMENT.
Si votre enfant présente des signes d'hypoglycémie pendant la prise d'Hemangiol, arrêtez le traitement et appelez immédiatement un médecin ou allez directement à l'hôpital. Si l'enfant est conscient, donnez-lui une boisson sucrée.
Risque de bronchospasme
Arrêtez le traitement et contactez immédiatement un médecin si, après avoir administré Hemangiol® à votre enfant, vous observez les symptômes suivants évocateurs d'un bronchospasme (rétrécissement temporaire des bronches entraînant des difficultés à respirer): toux, respiration rapide ou difficile ou sifflement respiratoire, associée ou non à une coloration bleuâtre de la peau.
Arrêtez le traitement et consultez immédiatement un médecin si votre enfant présente des symptômes de sensation de froid associés à des difficultés respiratoires et/ou un sifflement respiratoire lors de la prise d'HEMANGIOL.
Risque d'hypotension artérielle et de bradycardie (fréquence cardiaque anormalement basse)
Hemangiol peut diminuer la pression artérielle (hypotension) et la fréquence cardiaque (bradycardie). C'est pourquoi votre enfant sera gardé sous étroite surveillance clinique et monitorage de la fréquence cardiaque pendant 4 heures après la première dose ou après une augmentation de la dose. Par ailleurs, votre médecin examinera régulièrement votre enfant au cours du traitement.
Appelez immédiatement votre médecin si votre enfant présente des signes tels que fatigue, sensation de froid, pâleur, coloration bleuâtre de la peau ou évanouissement lors de la prise d'Hemangiol.
Risque d'hyperkaliémie
Hemangiol peut augmenter le taux sanguin de potassium (hyperkaliémie) en cas d'hémangiome ulcéré étendu. Dans ce cas, le taux sanguin de potassium de votre enfant devra être mesuré.
Si votre enfant doit subir une anesthésie générale
Votre enfant pourrait présenter une baisse de la pression artérielle s'il reçoit certains anesthésiques pendant la prise de ce médicament.
Il convient de prévenir l'anesthésiste que votre enfant est traité par Hemangiolet c'est à lui/elle de décider dans quel cas et pour combien de temps le traitement doit être interrompu avant l'intervention.
Autres médicaments et Hemangiol
- Informez votre médecin, pharmacien ou personnel médical si vous administrez, avez récemment administré ou pourriez administrer tout autre médicament à votre enfant. En effet, Hemangiol pourrait modifier la façon dont les autres médicaments agissent et certains médicaments pourraient avoir un effet sur la façon dont Hemangiol agit.
- Par ailleurs, si vous allaitez votre enfant, il est important de dire à votre médecin, votre pharmacien ou votre personnel médical quels médicaments vous prenez car ceux-ci pourraient passer dans votre lait et interférer avec le traitement de votre enfant. Votre médecin vous informera de la nécessité ou non d'interrompre l'allaitement.
En particulier, dans le cas où vous allaitez, informez votre médecin ou votre pharmacien si vous-même ou si votre enfant prenez/prend:
- des médicaments contre le diabète,
- des médicaments pour traiter des problèmes liés au cœur et aux vaisseaux sanguins, comme des battements irréguliers du cœur, des douleurs dans la poitrine ou une angine de poitrine, une hypertension artérielle, une insuffisance cardiaque,
- des médicaments pour traiter l'anxiété et la dépression ainsi que des problèmes de santé mentale plus graves ou une épilepsie,
- des médicaments pour traiter la tuberculose,
- des médicaments pour traiter la douleur et l'inflammation,
- des médicaments utilisés pour diminuer les lipides dans le sang,
- des médicaments utilisés pour l'anesthésie.
Si vous avez d'autres questions, interrogez votre médecin ou votre pharmacien.
Hemangiol contient moins de 1 mmol (23 mg) de sodium par flacon, c'est-à-dire qu'il est presque «sans sodium».
La dose maximale journalière d'Hemangiol contient 2,08 mg de propylène-glycol/kg/jour.
Si votre bébé a moins de 4 semaines, consultez votre médecin ou votre pharmacien avant de lui administrer ce médicament, en particulier si votre bébé reçoit simultanément d'autres médicaments contenant du propylène-glycol ou de l'alcool.
Hemangiol peut-il être pris/utilisé pendant la grossesse ou l’allaitement?
Si vous allaitez votre enfant:
- Informez votre médecin avant d'administrer ce médicament à votre enfant.
- N'administrez pas ce médicament à votre enfant si vous prenez des médicaments qui ne doivent pas être utilisés avec Hemangiol®.
Comment utiliser Hemangiol?
Le traitement de votre enfant a été débuté par un médecin qui est spécialiste du diagnostic, du traitement et de la prise en charge de l'hémangiome infantile.
Veillez à toujours administrer ce médicament en suivant exactement les indications de votre médecin ou de votre pharmacien. Vérifiez auprès de votre médecin ou de votre pharmacien en cas de doute.
Ne modifiez jamais vous-même la dose que vous administrez à votre enfant. Toute augmentation de la dose ou adaptation de la dose en fonction du poids de votre bébé doit être effectuée par votre médecin.
Posologie
La posologie est basée sur le poids de l'enfant selon le schéma ci-dessous:
Semaines | Dose par prise | Dose par prise | Moment de la prise |
Première semaine (1 mg/kg/jour ou 0,3 ml/kg) | 0,5 mg/kg | 0,15 ml/kg |
|
Deuxième semaine (2 mg/kg/jour ou 0,6 ml/kg) | 1 mg/kg | 0,3 ml/kg | |
Troisième semaine et semaines suivantes (3 mg/kg/jour ou 0,8 ml/kg) | 1,5 mg/kg | 0,4 ml/kg |
Comment administrer Hemangiol à votre enfant?
- Le médicament doit être administré pendant ou tout de suite après un repas.
- La dose doit toujours être mesurée à l'aide de la seringue pour administration orale fournie avec le flacon.
- Administrez Hemangiol directement dans la bouche de votre enfant à l'aide de la seringue pour administration orale fournie avec le flacon. Si nécessaire, vous pouvez mélanger le produit avec une petite quantité de lait pour bébé ou de jus de pomme et/ou d'orange adapté à l'âge de l'enfant et l'administrer à votre enfant dans un biberon. Ne mélangez pas le médicament dans un biberon plein de lait ou de jus.
Pour les enfants pesant jusqu'à 5 kg, vous pouvez mélanger la dose avec une cuillerée à café de lait (environ 5 ml). Pour les enfants pesant plus de 5 kg, la dose peut être mélangée avec une cuillerée à soupe de lait ou de jus de fruits (environ 15 ml).
Utilisez le mélange dans un délai de 2 heures suivant sa préparation.
- Nourrissez votre enfant régulièrement afin d'éviter un jeûne prolongé.
- Si votre enfant ne mange pas ou s'il vomit, il est recommandé de ne pas donner la dose.
- Si votre enfant recrache une dose ou si vous n'êtes pas sûr(e) qu'il a pris tout le médicament, ne lui administrez pas une autre dose, attendez la prochaine dose prévue.
- Hemangiol et le repas doivent être administrés par la même personne afin d'éviter le risque d'hypoglycémie. Si plusieurs personnes sont impliquées, une bonne communication est essentielle pour garantir la sécurité de votre enfant.
Respectez la posologie figurant sur la notice d'emballage ou prescrite par votre médecin. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l'efficacité du médicament est trop faible ou au contraire trop forte.
Instructions d'utilisation
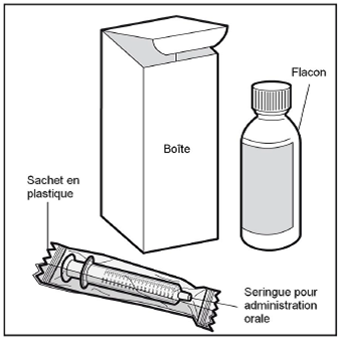
Étape 1: Retirer les éléments de la boîte
La boîte contient les éléments suivants dont vous aurez besoin pour administrer le médicament:
- le flacon en verre contenant 120 ml de propranolol solution buvable
- la seringue pour administration orale graduée en mg fournie avec ce médicament
Retirer le flacon d'Hemangiol et la seringue pour administration orale de la boîte et retirer la seringue du sachet en plastique.
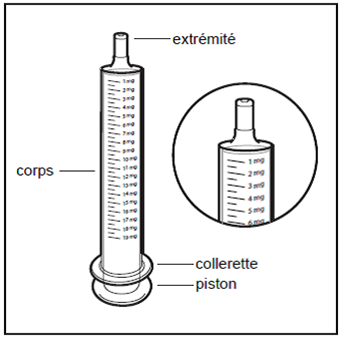
Étape 2: Vérifier la dose
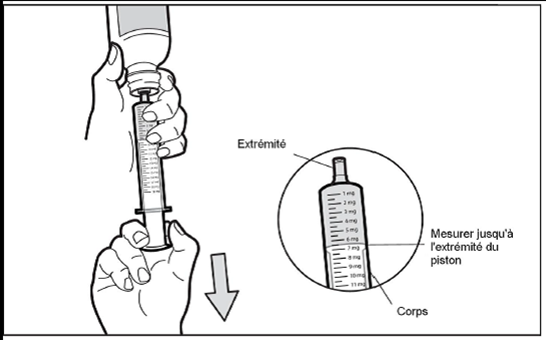
Vérifier la dose d'Hemangiol en milligrammes (mg) prescrite par le médecin de votre enfant. Repérer le chiffre sur la seringue pour administration orale.
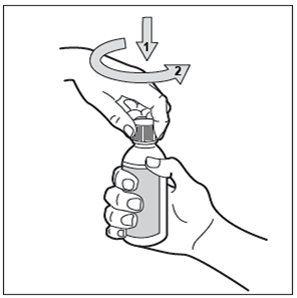
Étape 3: Ouvrir le flacon
Le flacon est muni d'un bouchon sécurité-enfant. Voici comment l'ouvrir: appuyer sur le bouchon en plastique tout en le tournant dans le sens contraire des aiguilles d'une montre (vers la gauche).
Ne pas agiter le flacon avant utilisation.
Étape 4: Introduire la seringue
Introduire l'extrémité de la seringue pour administration orale dans le flacon maintenu en position verticale et enfoncer complètement le piston.
Ne pas retirer l'adaptateur de la seringue du col du flacon.
Utiliser uniquement la seringue pour administration orale fournie avec le médicament pour mesurer et administrer la dose. Ne pas utiliser une cuillère ou tout autre dispositif de délivrance.
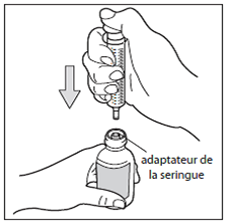
Étape 5: Prélever la dose
Avec la seringue pour administration orale en place, retourner le flacon, tête en bas.
Tirer le piston de la seringue jusqu'au nombre de mg dont vous avez besoin.
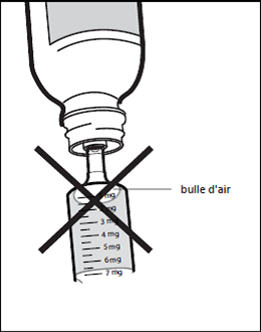
Étape 6: Vérifier les bulles d'air
Si vous voyez des bulles d'air dans la seringue pour administration orale, tenir la seringue en position droite, pousser le piston vers le haut suffisamment pour expulser complètement les grosses bulles d'air puis réajuster à la dose prescrite par votre médecin.
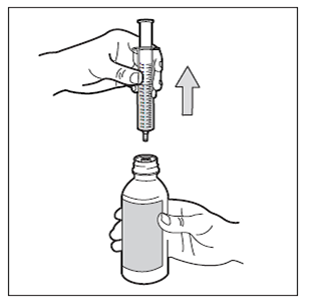
Étape 7: Retirer la seringue
Retourner le flacon en position verticale et retirer complètement la seringue du flacon. Veiller à ne pas appuyer sur le piston au cours de cette étape.
Étape 8: Fermer le flacon
Replacer le bouchon en plastique sur le flacon en le tournant dans le sens des aiguilles d'une montre (vers la droite).
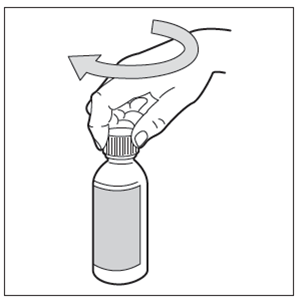
Étape 9: Administrer Hemangiol à votre enfant
Introduire la seringue dans la bouche de votre bébé et la placer contre l'intérieur de la joue.
Vous pouvez maintenant pousser lentement Hemangiol hors de la seringue directement dans la bouche de votre bébé.
Ne pas allonger l'enfant immédiatement après l'administration du médicament.
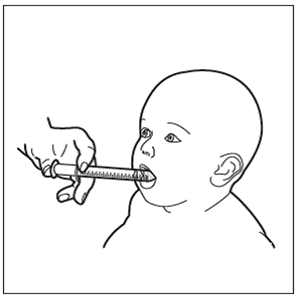
Étape 10: Nettoyer la seringue
Ne pas démonter la seringue. Rincer la seringue vide après chaque utilisation dans un verre d'eau propre:
- Prendre un verre d'eau propre
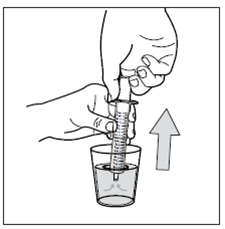
- Tirer le piston pour rincer la seringue
- Jeter l'eau dans l'évier
- Répéter ce processus de nettoyage 3 fois.
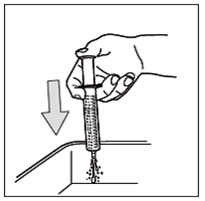
N'utiliser ni savon ni produit alcoolisé pour nettoyer la seringue. Essuyer l'extérieur de la seringue.
Ne pas placer la seringue dans un stérilisateur ou au lave-vaisselle.
Conserver le flacon et la seringue ensemble dans la boîte jusqu'à la prochaine utilisation, dans un lieu sûr où votre enfant ne peut pas les voir ou les prendre. Jeter la seringue lorsque le flacon est vide.
Si vous avez administré plus d'Hemangiol à votre enfant que vous n'auriez dû
Si vous avez administré plus d'Hemangiol à votre enfant que vous n'auriez dû, veuillez consulter immédiatement votre médecin.
Si vous oubliez d'administrer Hemangiol à votre enfant
N'administrez pas de dose double pour compenser la dose que vous avez oublié d'administrer. Poursuivez le traitement à la fréquence habituelle: une dose le matin et une dose en fin d'après-midi.
Si vous arrêtez d'administrer Hemangiol à votre enfant
Hemangiol peut être arrêté en une seule fois à la fin du traitement comme indiqué par le médecin.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d'informations à votre médecin, à votre pharmacien ou au personnel médical.
Respectez la posologie figurant sur la notice d'emballage ou prescrite par votre médecin. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l'efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Hemangiol peut-il provoquer?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, bien que tous n'y soient pas sujets.
Très fréquent (concerne plus d'un utilisateur sur 10)
- bronchite (inflammation des bronches),
- troubles du sommeil (insomnie, mauvaise qualité de sommeil et difficultés à se réveiller),
- diarrhée et vomissements.
Fréquent (concerne 1 à 10 utilisateurs sur 100')
- bronchospasme (difficultés à respirer),
- bronchiolite (inflammation des petites bronches avec des difficultés à respirer et un sifflement dans la poitrine associée à une toux et une fièvre),
- diminution de la pression artérielle,
- diminution de l'appétit,
- agitation, cauchemars, irritabilité,
- somnolence,
- extrémités froides,
- constipation, douleur abdominale,
- érythème (rougeur de la peau)
- érythème fessier.
Occasionnel (concerne 1 à 10 utilisateurs sur 1000)
- troubles de la conduction ou du rythme du cœur (battements cardiaques lents ou irréguliers),
- urticaire (réaction allergique de la peau), alopécie (perte de cheveux),
- diminution du taux de sucre dans le sang (hypoglycémie),
- réduction du nombre de globules blancs.
Fréquence indéterminée
- convulsions (crises convulsives) liées à une hypoglycémie (taux de sucre dans le sang anormalement bas),
- bradycardie (fréquence cardiaque anormalement basse),
- pression artérielle basse (hypotension),
- taux très faibles de globules blancs, les cellules chargées de combattre les infections,
- problèmes circulatoires qui entraînent un engourdissement et une pâleur des orteils et des doigts,
- taux élevé de potassium dans le sang.
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d'emballage.
À quoi faut-il encore faire attention?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Conserver le flacon dans l'emballage extérieur, hors de la vue et de la portée des enfants à une température ambiante (15-25 °C) et à l'abri de la lumière.
Le médicament ne doit pas être congelé.
Délai d'utilisation après ouverture: 2 mois
Ne pas agiter le flacon avant utilisation.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien qui disposent d'une information détaillée destinée aux professionnels.
Que contient Hemangiol?
1 ml d'Hemangiol, solution buvable contient:
Principes actifs
3,75 mg de propranolol base sous forme de 4,28 mg de chlorhydrate de propranolol.
Excipients
Arôme vanille et arôme fraise (contiennent du propylène-glycol), saccharine sodique, hydroxyéthylcellulose (produite à base de coton génétiquement modifié), acide citrique monohydraté, eau purifiée.
Numéro d’autorisation
61214 (Swissmedic).
Où obtenez-vous Hemangiol? Quels sont les emballages à disposition sur le marché?
En pharmacie, sur ordonnance médicale.
Flacon de 120 ml.
Titulaire de l'autorisation
Pierre Fabre (Suisse) SA, Allschwil.
Cette notice d'emballage a été vérifiée pour la dernière fois en septembre 2020 par l'autorité de contrôle des médicaments (Swissmedic).
Che cos'è Hemangiol e quando si usa?
Hemangiolsoluzione contiene il principio attivo propranololo. Il propranololo appartiene ad un gruppo di medamenti noti come betabloccanti. Questo medicamento è impiegato nel trattamento di emangiomi infantili in fase proliferativa che richiedono una terapia sistemica.
Il trattamento deve essere iniziato in bambini di età compresa tra 5 settimane e 5 mesi.
Un emangioma è costituito da un groviglio di vasi sanguigni che formano una piccola massa sulla cute o sotto di essa. L'emangioma può essere localizzato in superficie o in profondità. È talvolta denominato «voglia di fragola» perché la sua superficie ricorda un poco una fragola.
Quando non si può assumere/usare Hemangiol?
Non somministri Hemangiol se il suo bambino:
- è nato prematuro e non ha raggiunto l'età corretta di 5 settimane (l'età corretta è l'età che avrebbe un bambino prematuro se fosse nato alla data prevista del parto).
- pesa meno di 2 kg.
- è allergico al propranololo o ad uno qualsiasi degli altri componenti di questo medicamento. Una reazione allergica può manifestarsi ad es. con eruzioni cutanee, prurito o respiro affannoso.
- soffre di asma o ha avuto problemi respiratori in passato.
- presenta una frequenza cardiaca bassa per la sua età. In caso di dubbi, consulti il suo medico.
- ha problemi di cuore (ad es. disturbi del ritmo cardiaco o insufficienza cardiaca).
- presenta una pressione sanguigna molto bassa.
- presenta problemi di circolazione che rendono le dita dei piedi e delle mani fredde e pallide.
- tende ad avere bassi livelli di zucchero nel sangue.
- presenta una pressione sanguigna elevata causata da un tumore della ghiandola surrenale, denominato «feocromocitoma».
Se sta allattando il suo bambino con latte materno e se sta assumendo medicamenti che non devono essere usati in associazione con Hemangiol, NON somministri questo medicamento al suo bambino (cfr. la rubrica «Se sta allattando il suo bambino» e «Assunzione di Hemangiolcon altri medicamenti»).
Quando è richiesta prudenza nella somministrazione/nell’uso di Hemangiol?
Informi il medico o il farmacista prima di somministrare Hemangiolal suo bambino:
- Se il bambino ha problemi al fegato o ai reni. Questo medicamento non è raccomandato in caso di malattie epatiche o renali.
- Se il bambino ha avuto reazioni allergiche. Una reazione allergica può includere un'eruzione cutanea, prurito o respiro affannoso.
- Se il bambino soffre di psoriasi (condizione della pelle che si manifesta con placche rosse e secche di pelle ispessita), poiché questo medicamento può peggiorare i sintomi di questa malattia.
- Se il bambino ha il diabete: in questo caso, i livelli di glucosio nel sangue del suo bambino devono essere misurati con maggiore frequenza.
- Se il bambino è affetto dalla sindrome PHACE (condizione che associa emangiomi e anomalie cardiovascolari anche nei vasi sanguigni cerebrali), poiché questo medicamento può aumentare il rischio di ictus cerebrale.
Segnali importanti da tenere in considerazione dopo aver somministrato Hemangiol
Rischio di ipoglicemia
Questo medicamento può mascherare i sintomi premonitori dell'ipoglicemia (basso livello di zuccheri nel sangue). Può anche peggiorare l'ipoglicemia nei bambini, soprattutto durante il digiuno (ad es. scarsa assunzione di cibo per via orale, infezioni concomitanti, vomito), quando il fabbisogno di glucosio è aumentato (freddo, stress, infezioni) o in caso di sovradosaggio. Questi sintomi possono comprendere:
- Sintomi minori: pallore, stanchezza, sudorazione, tremori, palpitazioni, ansia, fame, difficoltà di risveglio.
- Sintomi maggiori: sonnolenza eccessiva, ridotta reattività, ridotta assunzione di cibo, calo della temperatura corporea, convulsioni (crisi), respirazione irregolare, perdita di conoscenza.
Per evitare un'ipoglicemia, somministrare HEMANGIOL durante o subito dopo un pasto ed evitare di somministrare l'ultima dose al bambino subito prima di metterlo a letto. Alimentare il bambino a sufficienza e con regolarità durante il trattamento. Se il suo bambino non mangia a sufficienza, presenta un altro disturbo o vomita, si raccomanda di saltare la dose. NON SOMMINISTRARE HEMANGIOL AL BAMBINO FINO A QUANDO NON SARÀ STATO DI NUOVO CORRETTAMENTE ALIMENTATO.
Se il suo bambino presenta sintomi di ipoglicemia mentre assume Hemangiol, interrompa il trattamento e consulti subito un medico o si rechi direttamente in ospedale. Se il bambino è cosciente, gli somministri un liquido orale contenente zucchero.
Rischio di broncospasmo
Interrompa il trattamento e contatti immediatamente un medico se, dopo aver somministrato Hemangiol, il suo bambino presenta i seguenti sintomi indicativi di broncospasmo (difficoltà respiratorie transitorie causate dal restringimento dei bronchi): tosse, respiro rapido o difficoltoso o ansimante, associati o meno a pelle di colore bluastro.
Se il suo bambino presenta sintomi simili al raffreddore associati a difficoltà respiratorie e/o respiro ansimante mentre assume HEMANGIOL, interrompa il trattamento e consulti subito un medico.
Rischio di ipotensione e bradicardia (bassa frequenza cardiaca)
Hemangiol può abbassare la pressione sanguigna (ipotensione) e la frequenza cardiaca (bradicardia). Per questa ragione, il bambino sarà tenuto sotto stretto monitoraggio clinico ed attenta osservazione della frequenza cardiaca per 4 ore dopo l'assunzione della prima dose o dopo un aumento del dosaggio. In seguito, il bambino sarà mantenuto sotto regolare controllo del medico durante il trattamento.
Contatti immediatamente il suo medico se il bambino mostra segni di stanchezza, freddo, pallore, pelle di colore bluastro o in caso di svenimento durante il trattamento con Hemangiol.
Rischio di iperkaliemia
Hemangiol può aumentare il livello di potassio nel sangue (iperkaliemia) in presenza di emangiomi ulcerati di ampie dimensioni. In questo caso è necessario misurare i livelli di potassio nel sangue del bambino.
Se il suo bambino deve essere sottoposto ad anestesia generale
Il suo bambino può presentare un calo della pressione sanguigna in caso di somministrazione di alcuni anestetici in contemporanea con l'assunzione di questo medicinale. Informi l'anestesista se il bambino assume Hemangiol. Questi deciderà se e per quanto tempo il trattamento con Hemangiol dovrà essere interrotto prima dell'intervento chirurgico.
Assunzione di Hemangiol con altri medicamenti
- Informi il medico, il farmacista o il personale medico se sta somministrando, ha recentemente somministrato o intende somministrare al bambino altri medicamenti. Hemangiol può influire sulla modalità d'azione di altri medicamenti e alcuni medicamenti possono influire sull'effetto di Hemangiol.
- Inoltre, se sta allattando con latte materno, è importante informare il medico, il farmacista o il personale medico dei medicamenti che lei sta assumendo poiché questi potrebbero passare nel latte e interferire con il trattamento del bambino. Il medico le dirà se interrompere o meno l'allattamento.
Informi il suo medico o il farmacista se il suo bambino sta assumendo altri medicamenti, in particolare:
- Medicamenti per il diabete,
- Medicamenti per il trattamento di problemi di cuore o vascolari, come ad es. battito irregolare, dolore al petto o angina, pressione sanguigna alta, insufficienza cardiaca,
- Medicamento per il trattamento dell'ansia e della depressione, per problemi psichiatrici più gravi e per l'epilessia,
- Medicamenti per il trattamento della tubercolosi,
- Medicamenti antidolorifici e antinfiammatori,
- Medicamenti per abbassare i grassi nel sangue,
- Medicamenti anestetici.
Per ulteriori domande, si rivolga al suo medico o al farmacista.
Hemangiol contiene meno di 1 mmol (23 g) di sodio per flacone, cioè è essenzialmente «senza sodio».
La dose massima giornaliera di Hemangiol contiene 2,08 g di propilene glicole/kg/giorno.
Se il bambino ha meno di 4 settimane di età, parli con il medico o il farmacista prima di somministrare questo medicamento, in particolare se il bambino sta assumendo altri medicinali contenenti propilene glicole o alcol.
Si puo assumere/usare Hemangiol durante la gravidanza o l’allattamento?
Se sta allattando il suo bambino:
- Informi il suo medico prima che le prescriva questo medicamento.
- Non somministri questo medicamento al suo bambino se sta assumendo medicamenti che non devono essere usati insieme a Hemangiol®.
Come usare Hemangiol?
Il trattamento del bambino è stato iniziato da un medico esperto in materia di diagnosi e trattamento degli emangiomi infantili.
Somministri questo medicamento al suo bambino seguendo sempre esattamente le istruzioni del medico o del farmacista. In caso di dubbi, consulti il suo medico o il farmacista.
Non modifichi mai di propria iniziativa la dose somministrata al bambino. Ogni aumento o aggiustamento della dose in base al peso del bambino deve essere prescritto dal medico.
Posologia
La posologia si basa sul peso del bambino, come illustrato nello schema seguente:
Settimane | Dose per somministrazione | Dose per somministrazione | Tempi di somministrazione |
Prima settimana (1 mg/kg/giorno o 0,3 ml/kg) | 0,5 mg/kg | 0,15 ml/kg |
|
Seconda settimana (2 mg/kg/giorno o 0,6 ml/kg) | 1 mg/kg | 0,3 ml/kg | |
Terza settimana e successive (3 mg/kg/giorno o 0,8 ml/kg) | 1,5 mg/kg | 0,4 ml/kg |
Come somministrare Hemangiol al suo bambino?
- Il medicamento deve essere somministrato durante o subito dopo un pasto.
- La dose deve essere sempre misurata con l'ausilio della siringa per uso orale fornita con il flacone.
- Somministri Hemangiol direttamente nella bocca del bambino utilizzando la siringa per uso orale fornita insieme al flacone. Se necessario, può miscelare il prodotto in una piccola quantità di latte per neonati o di succo di mela e/o d'arancia adatto all'età del bambino e lo somministri al bambino con il biberon. Non metta il medicamento in una bottiglia piena di latte o di succo.
- Per i bambini fino a 5 kg di peso, la dose può essere miscelata con un cucchiaino di latte (circa 5 ml). Per bambini di peso superiore a 5 kg, la dose può essere miscelata con un cucchiaio di latte o di succo di frutta (circa 15 ml).
Usare la miscela entro 2 ore.
- Alimenti il bambino regolarmente, per evitare digiuni prolungati.
- Se il bambino non mangia o vomita, si raccomanda di saltare la dose.
- Se il bambino vomita la dose o se non è certo che abbia assunto tutto il medicamento, non somministri un'altra dose ma attenda la dose successiva prevista.
- Hemangiol e i pasti devono essere somministrati dalla stessa persona per evitare il rischio di ipoglicemia. Se persone diverse si occupano del bambino, la comunicazione è fondamentale per garantire la sicurezza del bambino.
Si attenga alla posologia indicata nel foglietto illustrativo o prescritta dal suo medico. Se ritiene che l'azione del medicamento sia troppo debole o troppo forte ne parli al suo medico o al suo farmacista.
Istruzioni per l'uso:
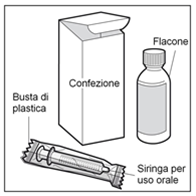
Fase 1: Estrarre gli articoli dalla confezione
La confezione contiene i seguenti articoli che serviranno per somministrare il medicamento:
- un flacone in vetro contenente 120 ml di propranololo, soluzione orale
- una siringa per uso orale graduata in mg fornita con il medicamento
Estrarre il flacone e la siringa per uso orale dalla confezione ed estrarre la siringa dalla busta di plastica.
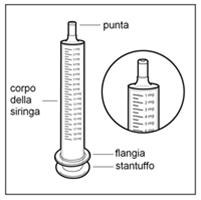
Fase 2: Controllare la dose
Controllare la dose di Hemangiol in milligrammi (mg) come prescritto dal medico. Individuare il numero corrispondente sulla siringa per uso orale.
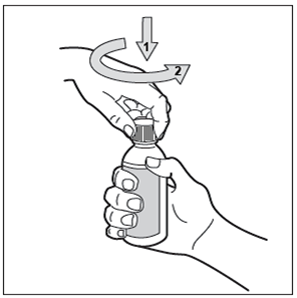
Fase 3: Aprire il flacone
Il flacone è dotato di tappo a prova di bambino. Per aprire il flacone, premere il tappo di plastica verso il basso e ruotarlo in senso antiorario (verso sinistra).
Non agitare il flacone prima dell'uso.
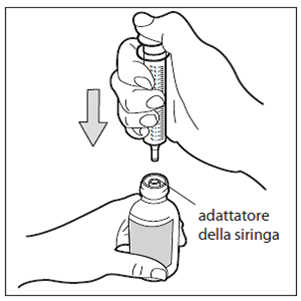
Fase 4: Inserire la siringa
Mantenendo il flacone in posizione verticale, inserire la punta della siringa per uso orale nel flacone e spingere lo stantuffo completamente verso il basso.
Non rimuovere l'adattatore della siringa dal collo del flacone.
Per misurare e somministrare la dose, utilizzare unicamente la siringa per uso orale fornita con il medicamento. Non utilizzare cucchiai o altri dispositivi di somministrazione.
Fase 5: Estrarre la dose
Con la siringa per uso orale inserita, capovolgere il flacone.
Tirare lo stantuffo della siringa fino al numero di mg richiesti.
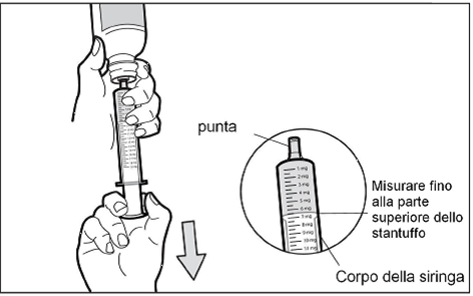
Fase 6: Controllare l'assenza di bolle d'aria
Se la siringa contiene bolle d'aria, mantenere la siringa verticale, spingere lo stantuffo verso l'alto quanto basta per eliminare completamente tutte le bolle d'aria di grandi dimensioni e quindi riportarlo alla dose prescritta dal medico.
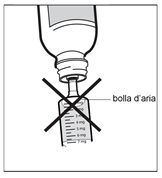
Fase 7: Rimuovere la siringa
Riportare il flacone in posizione verticale e rimuovere completamente la siringa dal flacone. Fare attenzione a non spingere lo stantuffo durante questa operazione.
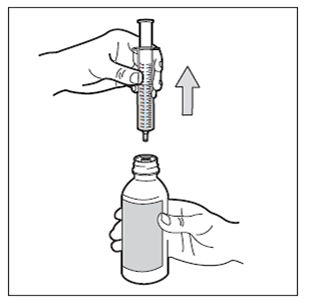
Fase 8: Chiudere il flacone.
Riposizionare il tappo di plastica sul flacone ruotandolo in senso orario (verso destra).
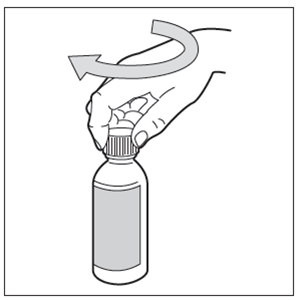
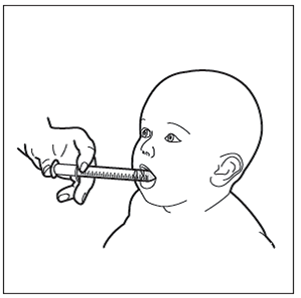
Fase 9: Somministrare Hemangiol al bambino
Inserire la siringa nella bocca del bambino e posizionarla contro la parete interna della guancia.
Iniettare lentamente Hemangiol dalla siringa direttamente nella bocca del bambino.
Non fare sdraiare il bambino subito dopo aver somministrato il medicamento.
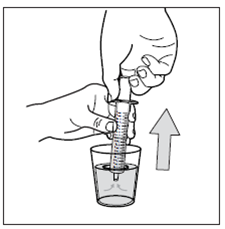
Fase 10: Ripulire la siringa.
Non smontare la siringa. Sciacquare la siringa vuota dopo ogni utilizzo lavandola in un bicchiere d'acqua:
- Riempire un bicchiere d'acqua pulita
- Tirare lo stantuffo
- Svuotare l'acqua nel lavandino
- Ripetere questa operazione di pulitura per 3 volte.
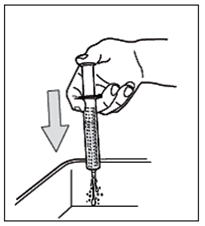
Non usare prodotti detergenti o a base di alcool per pulire la siringa. Asciugare la parte esterna.
Non mettere la siringa in uno sterilizzatore o in lavastoviglie.
Riporre il flacone e la siringa insieme nella scatola di cartone fino all'uso successivo, conservandoli in un luogo sicuro lontano dalla vista e dalla portata del bambino. Gettare la siringa una volta esaurito il contenuto del flacone.
Se il bambino assume una dose di Hemangiol superiore al necessario
Se ha somministrato al bambino una dose di Hemangiol superiore alla dose prevista, consulti immediatamente il suo medico.
Se dimentica di somministrare Hemangiol al bambino
Non somministri una dose doppia per compensare la dimenticanza della dose. Continui il trattamento con la dose successiva prevista secondo la normale frequenza: una dose al mattino e una nel tardo pomeriggio.
Se interrompe la somministrazione di Hemangiol al bambino
La somministrazione di Hemangiol può essere interrotta immediatamente al termine del trattamento, come stabilito dal medico.
Per ulteriori domande sull'uso di questo medicamento, si rivolga al medico, al farmacista o al personale medico.
Si attenga alla posologia indicata nel foglietto illustrativo o prescritta dal suo medico. Se ritiene che l'azione del medicamento sia troppo debole o troppo forte ne parli al suo medico o al suo farmacista.
Quali effetti collaterali può avere Hemangiol?
Come tutti i medicamenti, questo medicamento può causare effetti indesiderati sebbene non tutte le persone li manifestino.
Molto comune (riguarda più di 1 utilizzatore su 10)
- Bronchite (infiammazione dei bronchi)
- Disturbi del sonno (insonnia, scarsa qualità del sonno e difficoltà di risveglio)
- Diarrea e vomito
Comune (riguarda da 1 a 10 utilizzatori su 100)
- Broncospasmo (difficoltà respiratorie)
- Bronchiolite (infiammazione dei bronchioli accompagnata da difficoltà respiratorie e sibilo nel petto), associata a tosse e febbre
- Pressione sanguigna ridotta
- Appetito ridotto
- Agitazione, incubi, irritabilità
- Sonnolenza
- Estremità fredde
- Stipsi, dolore addominale
- Eritema (arrossamento cutaneo)
- Eritema da pannolino
Non comune (riguarda da 1 a 10 utilizzatori su 1000)
- Disturbi della conduzione cardiaca o del ritmo (battiti lenti o irregolari)
- Orticaria (reazione allergica delle pelle), alopecia (perdita dei capelli)
- Livelli ridotti di zuccheri nel sangue
- Riduzione del numero di globuli bianchi
Frequenza non nota
- Convulsioni (crisi) legate all'ipoglicemia (livello di zuccheri nel sangue eccessivamente basso)
- Bradicardia (frequenza cardiaca eccessivamente bassa)
- Bassa pressione sanguigna
- Forte riduzione del numero dei globuli bianchi, che combattono le infezioni
- Problemi circolatori che rendono le dita delle mani e dei piedi fredde e pallide
- Livelli aumentati di potassio nel sangue
Se osserva effetti collaterali, si rivolga al suo medico o farmacista, soprattutto se si tratta di effetti collaterali non descritti in questo foglietto illustrativo.
Di che altro occorre tener conto?
Il medicamento non dev'essere utilizzato oltre la data indicata con «EXP» sul contenitore.
Hemangiol deve essere conservato ben chiuso nella confezione originale e fuori dalla portata dei bambini, a temperatura ambiente (15-25 °C) e al riparo dalla luce.
Termine di consumo dopo l'apertura: 2 mesi.
Non agitare il flacone prima dell'uso.
Il medico o il farmacista, che sono in possesso di un'informazione professionale dettagliata, possono darle ulteriori informazioni.
Cosa contiene Hemangiol?
1 ml di Hemangiol, soluzione orale contiene
Principi attivi
3,75 mg di propranololo (base) sotto forma di 4,28 mg di propranololo cloridrato.
Sostanze ausiliarie
Aroma di vaniglia e aroma di fragola (contengono propilene glicole), saccarina sodica, idrossietilcellulosa (prodotta da cotone geneticamente modificato), acido citrico monoidrato, acqua purificata.
Numero dell’omologazione
61214 (Swissmedic)
Dove è ottenibile Hemangiol? Quali confezioni sono disponibili?
In farmacia, dietro presentazione della prescrizione medica.
Flacone da 120 ml
Titolare dell’omologazione
Pierre Fabre (Suisse) S.A., 4123 Allschwil
Questo foglietto illustrativo è stato controllato l'ultima volta nel settembre 2020 dall'autorità competente in materia di medicamenti (Swissmedic).
Zusammensetzung
Wirkstoffe
Propranolol als Propranololhydrochlorid.
Hilfsstoffe
Vanillearoma und Erdbeeraroma (enthalten 2.6 mg/ml Propylenglycol), Saccharin-Natrium (enthält 0.17 mg/ml Natrium), Hydroxyethylcellulose (aus gentechnisch veränderter Baumwolle hergestellt), Citronensäure-Monohydrat, gereinigtes Wasser.
Darreichungsform und Wirkstoffmenge pro Einheit
1 ml Lösung zum Einnehmen enthält 3,75 mg Propranolol (Base) als 4,28 mg Propranololhydrochlorid.
Indikationen/Anwendungsmöglichkeiten
Hemangiol ist zur Behandlung proliferativer infantiler Hämangiome, die eine systemische Therapie erfordern, angezeigt.
Die Therapie wird bei Säuglingen zwischen 5 Wochen und 5 Monaten begonnen.
Dosierung/Anwendung
Die Behandlung mit HEMANGIOL sollte von Ärzten, die über Erfahrung in Diagnose, Behandlung und Management des infantilen Hämangioms verfügen, in einem kontrollierten klinischen Umfeld mit angemessenen Einrichtungen zur Handhabung unerwünschter Reaktionen, einschliesslich solcher, die Notfallmassnahmen erfordern, initiiert werden.
Dosierung
Die Dosierung wird in Propranolol (Base) angegeben.
Die empfohlene Anfangsdosis beträgt 1 mg/kg/Tag, die in zwei separate Dosen zu 0,5 mg/kg aufgeteilt wird. Wenn der Patient das Medikament gut verträgt, kann die Dosis nur unter ärztlicher Aufsicht erhöht werden. Die Dosiserhöhung ist wie folgt vorzunehmen: 1 Woche lang 1 mg/kg/Tag, anschliessend 1 Woche lang 2 mg/kg/Tag und dann 3 mg/kg/Tag als Erhaltungsdosis.
Die therapeutische Dosis beträgt 3 mg/kg/Tag, die in 2 gleichen, separaten Dosen zu 1,5 mg/kg einmal morgens und einmal am späten Nachmittag zu verabreichen ist. Zwischen den beiden Einnahmen muss ein zeitlicher Abstand von mindestens 9 Stunden liegen. Das Arzneimittel ist während oder kurz nach einer Nahrungsaufnahme einzunehmen.
Um dem Risiko einer Hypoglykämie vorzubeugen, ist Hemangiol während oder unmittelbar nach einer Nahrungsaufnahme zu verabreichen. Wenn das Kind nichts zu sich nimmt oder erbricht, wird empfohlen, die Dosis auszulassen.
Sollte das Kind eine Dosis ausspucken oder das Arzneimittel nicht vollständig aufnehmen, ist vor der nächsten vorgesehenen Dosis keine weitere Dosis zu verabreichen.
Während der Aufdosierung muss jede Dosiserhöhung unter den gleichen Bedingungen wie die Verabreichung der Anfangsdosis von einem Arzt angeleitet und überwacht werden. Nach der Aufdosierung wird der Arzt die Dosis entsprechend den Gewichtsveränderungen beim Kind neu anpassen (siehe Tabelle 1).
Tabelle 1. Dosierung in Abhängigkeit vom Gewicht
Woche 1 | Woche 2 | Woche 3 (Erhaltung) | |
|---|---|---|---|
Gewicht (kg) | Dosis zweimal am Tag gegeben | ||
2 bis <2.5 | 1 mg | 2 mg | 3 mg |
2.5 bis <3 | 1 mg | 2.5 mg | 3.5 mg |
3 bis <3.5 | 1.5 mg | 3 mg | 4.5 mg |
3.5 bis <4 | 1.5 mg | 3.5 mg | 5 mg |
4 bis <4.5 | 2 mg | 4 mg | 6 mg |
4.5 bis <5 | 2 mg | 4.5 mg | 6.5 mg |
5 bis <5.5 | 2.5 mg | 5 mg | 7.5 mg |
5.5 bis <6 | 2.5 mg | 5.5 mg | 8 mg |
6 bis <6.5 | 3 mg | 6 mg | 9 mg |
6.5 bis <7 | 3 mg | 6.5 mg | 9.5 mg |
7 bis <7.5 | 3.5 mg | 7 mg | 10.5 mg |
7.5 bis <8 | 3.5 mg | 7.5 mg | 11 mg |
8 bis <8.5 | 4 mg | 8 mg | 12 mg |
8.5 bis <9 | 4 mg | 8.5 mg | 12.5 mg |
9 bis <9.5 | 4.5 mg | 9 mg | 13.5 mg |
9.5 bis <10 | 4.5 mg | 9.5 mg | 14 mg |
10 bis <10.5 | 5 mg | 10 mg | 15 mg |
10.5 bis <11 | 5 mg | 10.5 mg | 15.5 mg |
11 bis <11.5 | 5.5 mg | 11 mg | 16.5 mg |
11.5 bis <12 | 5.5 mg | 11.5 mg | 17 mg |
12 bis <12.5 | 6 mg | 12 mg | 18 mg |
Die klinische Überwachung des Gesundheitszustands des Kindes sowie eine Neuanpassung der Dosis muss mindestens einmal pro Monat durchgeführt werden.
Dauer der Behandlung
Hemangiol ist über einen Zeitraum von 6 Monaten anzuwenden. Beim Absetzen der Behandlung ist es nicht nötig, die Dosis schrittweise zu reduzieren.
Bei der Minderheit der Patienten, die nach Absetzen der Behandlung ein Rezidiv der Symptome zeigen, kann die Behandlung unter denselben Bedingungen erneut begonnen.
Spezifische Populationen
Hemangiol darf nicht bei Kindern unter 5 Wochen angewendet werden, da bei dieser Patientengruppe keine Daten zur klinischen Wirksamkeit und Sicherheit vorliegen. Es liegen aus klinischen Studien mit Hemangiol keine Daten zur klinischen Wirksamkeit und Sicherheit vor, daher ist eine Erstbehandlung von Säuglingen und Kindern über 5 Monaten nicht zu empfehlen.
Säuglinge mit Leber- oder Nierenfunktionsstörung:
Da keine Daten vorliegen, ist die Verabreichung des Arzneimittels an Säuglinge mit eingeschränkter Leber- und Nierenfunktion nicht empfohlen.
Art der Anwendung
Hemangiol muss mittels einer graduierten Oralspritze direkt in den Mund des Kindes verabreicht werden. Die Spritze liegt der Flasche mit der Lösung zum Einnehmen bei und ist für Milligramm Propranolol (Base) kalibriert.
Die Flasche sollte vor der Verwendung nicht geschüttelt werden.
Falls nötig kann das Arzneimittel in einer kleinen Menge Säuglingsmilch oder altersgerechtem Apfel- und/oder Orangensaft verdünnt werden. Das Arzneimittel darf nicht in die volle Flasche gegeben werden.
Das Arzneimittel kann für Kinder mit einem Gewicht von bis zu 5 kg mit einem Teelöffel (ungefähr 5 ml) Milch gemischt werden, für Kinder mit einem Gewicht von mehr als 5 kg mit einem Esslöffel (ungefähr 15 ml) Milch oder Fruchtsaft. Die Mischung kann in eine Babyflasche verabreicht werden. Die Mischung sollte innerhalb von 2 Stunden verwendet werden.
Um das Risiko einer Hyperglykämie auszuschalten, müssen Hemangiol und die Nahrung von derselben Person gegeben werden. Wenn verschiedene Personen einbezogen sind, ist eine gute Kommunikation unabdingbar, um die Sicherheit des Kindes zu gewährleisten.
Kontraindikationen
- Frühgeborene, bei denen das korrigierte Alter von 5 Wochen noch nicht erreicht ist (das korrigierte Alter wird errechnet, indem man die Anzahl der Wochen, die das Kind zu früh geboren wurde, vom tatsächlichen Alter abzieht)
- Gewicht < 2kg
- Gestillte Kinder, deren Mutter mit Arzneimitteln behandelt wird, die nicht zusammen mit Propranolol angewendet werden dürfen
- Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile
- Asthma oder anamnestisch bekannter Bronchospasmus
- Atrioventrikulärer Block 2. oder 3. Grades
- Erkrankung des Sinusknotens (einschliesslich sinuatrialer Block)
- Bradykardie unterhalb folgender Grenzwerte:
Alter | 0-3 Monate | 3-6 Monate | 6-12 Monate |
|---|---|---|---|
Herzfrequenz | 100 | 90 | 80 |
- Niedriger Blutdruck unterhalb folgender Grenzwerte:
Alter | 0-3 Monate | 3-6 Monate | 6-12 Monate |
|---|---|---|---|
Blutdruck (mmHg) | 65/45 | 70/50 | 80/55 |
- Kardiogener Schock
- Nicht medikamentös kontrollierte Herzinsuffizienz
- Prinzmetal-Angina
- Schwere periphere arterielle Kreislaufstörungen (Raynaud-Syndrom)
- Kleinkinder mit Hypoglykämieneigung
- Phäochromozytom
Warnhinweise und Vorsichtsmassnahmen
Beginn der Therapie
Vor Beginn der Therapie mit Propranolol müssen die mit der Anwendung dieses Wirkstoffs verbundenen Risiken abgeklärt werden. Die Anamnese muss ausgewertet werden und es muss eine vollständige klinische Untersuchung erfolgen, einschliesslich Messung der Herzfrequenz sowie Abhören von Herz und Lunge.
Falls eine Herzanomalie vermutet wird, muss vor Beginn der Behandlung der Rat eines Spezialisten eingeholt werden, um alle zugrundeliegenden Kontraindikationen zu bestimmen.
Im Falle einer akuten broncho-pulmonalen Anomalie ist der Behandlungsbeginn aufzuschieben.
Hypoglykämie
Propranolol verhindert die Reaktion auf endogene Katecholamine, die normalerweise einer Hypoglykämie entgegenwirken. Das Arzneimittel maskiert die adrenergen Warnzeichen einer Hypoglykämie, insbesondere Tachykardie, Zittrigkeit, Angst und Hunger. Es kann eine Hypoglykämie bei Kindern verschlimmern, speziell in Fastensituationen (z.B. bei nicht erfolgter Nahrungsaufnahme, Infektionen, Erbrechen), bei erhöhtem Glukosebedarf (Erkältung, Stress, Infektionen) oder im Falle einer Überdosierung.
Diese hypoglykämischen Episoden im Zusammenhang mit der Einnahme von Propranolol können sich in Ausnahmefällen in Form von Krampfanfällen und/oder Koma manifestieren.
Bei Auftreten der klinischen Anzeichen einer Hypoglykämie muss dem Kind eine zuckerhaltige Lösung zu trinken gegeben und die Behandlung vorübergehend unterbrochen werden. Bis zum Verschwinden der Symptome muss das Kind entsprechend überwacht werden.
Die verschreibende Ärztin/der verschreibende Arzt sollte die pflegenden Angehörigen/Eltern über das Risiko einer schweren Hypoglykämie informieren, dass während der gesamten Behandlungsdauer gleich stark ausgeprägt bleibt, und die Notwendigkeit betonen, die Dosierungsempfehlungen einzuhalten (siehe Abschnitt Dosierung/Anwendung).
Pflegende sollten eine Anleitung erhalten, wie sie die klinischen Anzeichen einer Hypoglykämie erkennen können, um
- einen hypoglykämischen Zustand sofort zu behandeln und lebensbedrohliche Situationen zu vermeiden,
- einen Arzt zu kontaktieren oder direkt ins Krankenhaus zu gehen,
- die Behandlung einzustellen.
Bei Kindern mit Diabetes sollte der Blutzucker häufiger überwacht und von einem Endokrinologen kontrolliert werden.
Gleichzeitige Verabreichung von Propranolol mit Kortikosteroiden kann das Risiko von Hypoglykämie erhöhen.
Erkrankungen der Atemwege
Im Falle einer Infektion der unteren Atemwege, die mit Atemnot und pfeifender oder keuchender Atmung einhergeht, ist die Behandlung vorübergehend abzusetzen. Es können Beta-2-Agonisten und inhalierbare Kortikosteroide angewendet werden. Eine erneute Verabreichung von Propranolol unter ärztlicher Aufsicht kann erwogen werden, wenn das Kind vollständig genesen ist; bei einem erneuten Auftreten der Atemwegserkrankung ist die Behandlung dauerhaft abzusetzen.
Im Falle eines isolierten Bronchospasmus muss die Behandlung ebenfalls dauerhaft abgesetzt werden.
Kardiovaskuläre Erkrankungen
Aufgrund seiner pharmakologischen Wirkung kann Propranolol eine Bradykardie oder Blutdruckstörungen auslösen oder verschlimmern. Eine Bradykardie ist zu diagnostizieren, wenn die Herzfrequenz um mehr als 30 bpm gegenüber dem Ausgangswert sinkt. Bradykardie ist definiert als eine Herzfrequenz unter den folgenden Grenzwerten:
Alter | 0-3 Monate | 3-6 Monate | 6-12 Monate |
|---|---|---|---|
Herzfrequenz | 100 | 90 | 80 |
Nach der ersten Einnahme und jeder Dosiserhöhung sind mindestens 4 Stunden lang eine klinische Überwachung, einschliesslich Blutdruck und Herzfrequenz vorzunehmen. Falls eine symptomatische Bradykardie oder Bradykardie unter 80 bpm, ist sofort der Rat eines Spezialisten einzuholen.
Falls zu einem beliebigen Zeitpunkt während der Behandlung eine schwere und/oder symptomatische Bradykardie oder Hypotonie auftritt, ist die Behandlung abzusetzen und der Rat eines Spezialisten einzuholen.
Herzinsuffizienz
Bei Patienten mit kongestiver Herzinsuffizienz stellt die sympathische Stimulation möglicherweise eine entscheidende Komponente zur Unterstützung der Kreislauffunktion dar. Folglich könnte sich eine Hemmung dieser Stimulation durch Betablockade in einer stärkeren Insuffizienz niederschlagen. Bei Kindern mit Herzinsuffizienz sollte die Behandlung durch einen Kardiologen geleitet werden.
PHACE-Syndrom
Es liegen nur sehr wenige Sicherheitsdaten zu Propranolol bei Patienten mit PHACE-Syndrom vor.
Durch den Blutdruckabfall und die Verminderung des Blutflusses durch verstopfte, enge oder von Stenose betroffene Gefässe könnte Propranolol bei Patienten mit PHACE-Syndrom und schweren zerebrovaskulären Anomalien das Schlaganfallrisiko erhöhen.
Vor der Entscheidung über eine Therapie mit Propranolol sind Säuglinge mit einem grossen infantilen Hämangiom im Gesichtsbereich gründlich auf eine mögliche Arteriopathie im Zusammenhang mit dem PHACE-Syndrom zu untersuchen. Dabei müssen eine Magnetresonanzangiographie von Kopf und Hals sowie ein bildgebendes Verfahren zur Darstellung des Herzens unter Einbeziehung des Aortenbogens durchgeführt werden.
Der Rat eines Spezialisten ist einzuholen.
Stillzeit
Propranolol geht in die Muttermilch über. Frauen, die mit Propranolol behandelt werden und ihr Kind stillen, müssen ihren Arzt bzw. Ärztin informieren.
Leber- oder Nierenversagen
Propranolol wird in der Leber metabolisiert und über die Nieren ausgeschieden. Da zu Kindern keine Daten vorliegen, wird Propranolol bei Nieren- oder Leberfunktionsstörung nicht empfohlen.
Überempfindlichkeit
Bei Patienten, bei denen wahrscheinlich eine schwere anaphylaktische Reaktion, unabhängig von der Ursache und insbesondere mit jodhaltigen Kontrastmitteln, auftritt, kann eine Behandlung mit Betarezeptorenblockern zu einer Verstärkung der Reaktion und einer Resistenz gegenüber der Behandlung mit Adrenalin in normaler Dosierung führen. Im Falle eines erhöhten Anaphylaxie Risikos, sollte dieses in die Nutzen-Risiko Bewertung zur Anwendung von Hemangiol einfliessen.
Hemangiol enthält weniger als 1 mmol Natrium (23 mg) pro Flasche, d.h. es ist im Wesentlichen «natriumfrei».
Die maximale tägliche Dosis Hemangiol enthält 2,08 mg Propylenglykol/kg/Tag. Die gleichzeitige Anwendung mit einem Substrat der Alkoholdehydrogenase – wie Ethanol – kann schwerwiegende Nebenwirkungen bei Neugeborenen hervorrufen.
Vollnarkose
Betarezeptorenblocker führen zu einer Abschwächung der Reflextachykardie und einem erhöhten Hypotonierisiko. Der Anästhesist bzw. Anästhesistin muss über die Behandlung des Patienten mit Betarezeptorenblockern informiert werden und sie/er wird entscheiden, ob und für wie lange die Behandlung mit Betarezeptorenblockern vor dem chirurgischen Eingriff abgesetzt wird.
Hyperkaliämie
Bei Patienten mit grossen ulzerierten Hämangiomen traten Fälle von Hyperkaliämie auf. Bei diesen Patienten ist eine Überwachung der Elektrolyte angezeigt.
Psoriasis
Bei Patienten, die unter Psoriasis leiden, wurde unter Betarezeptorenblockern über eine Verschlechterung der Krankheit berichtet. Die Notwendigkeit der Behandlung ist daher sorgfältig abzuwägen.
Interaktionen
Da keine spezifischen Studien an Kindern durchgeführt wurden, handelt es sich hierbei um die bei Erwachsenen bekannten Arzneimittelwechselwirkungen mit Propranolol. In folgenden beiden Situationen sind Kombinationen zu berücksichtigen:
- Säuglinge, die mit einem der im Folgenden aufgeführten Arzneimitteln behandelt werden
- Gestillte Kinder, deren Mutter eines der folgenden oder andere Arzneimittel einnimmt bzw. anwendet. Im letzteren Fall ist abzuwägen, ob das Stillen unterbrochen werden muss.
- Eine engmaschige klinische Überwachung jeglicher eingeschränkten Toleranz gegenüber Propranolol ist angezeigt.
Einfluss von Propranolol auf gleichzeitig verabreichte Arzneimittel:
Der Einfluss von Propranolol auf die Plasmakonzentration von gleichzeitig verabreichten Arzneimitteln, ist in der unten aufgeführten Tabelle dargestellt:
Gleichzeitig verabreichtes Arzneimittel | Einfluss auf die Plasma- Konzentration gleichzeitig verabreichter Arzneimittel |
|---|---|
Amid-anästhetika (Lidocain, Bupivacain, Mepivacain) | Anstieg |
Warfarin | Anstieg |
Propafenon | Anstieg > 200% |
Nifedipin | Anstieg 80% |
Verapamil | Unverändert |
Pravastatin, lovastatin | Abnahme 20% |
Fluvastatin | Unverändert |
Zolmitriptan | Anstieg 60% |
Rizatriptan | Anstieg 80% |
Thioridazin | Anstieg 370% |
Diazepam | Anstieg |
Oxazepam, Triazolam, Lorazepam, Alprazolam | Unverändert |
Theophyllin | Anstieg 70% |
Einfluss von gleichzeitig verabreichten Arzneimitteln auf Propranonol:
Der Einfluss von gleichzeitig verabreichten Arzneimitteln auf die Plasma-Konzentration von Propranolol, ist in der unten aufgeführten Tabelle dargestellt:
Gleichzeitig verabreichtes Arzneimittel | Einfluss auf die Plasma-Konzentration von Propranolol |
|---|---|
CYP2D6, CYP1A2 oder CYP2C19 Inhibitoren | Anstieg |
CYP1A2 oder CYP2C19 Induktoren | Abnahme |
Quinidin | Anstieg > 200% |
Nisoldipin | Anstieg 50% |
Nicardipin | Anstieg 80% |
Chlorpromazin | Anstieg 70% |
Cimetidin | Anstieg 50% |
Cholestyramin, colestipol | Abstieg 50% |
Alkohol | Anstieg (Akut), Abnahme (Chronisch) |
Diazepam | Unverändert |
Verapamil | Unverändert |
Metoclopramid | Unverändert |
Ranitidin | Unverändert |
Lansoprazol | Unverändert |
Omeprazol | Unverändert |
Propafenon | Anstieg 200% |
Aluminumhydroxid | Abnahme 50% |
Nicht empfohlene gleichzeitige Anwendung
Bradykardie –induzierende Calciumkanalblocker (Diltiazem, Verapamil, Bepridil)
Die gleichzeitige Gabe von Propranolol kann zu einem veränderten Automatismus (übermäβige Bradykardie, Sinusarrest), sinoatrialen und atrioventrikulären Überleitungsstörungen sowie einem erhöhten Risiko für mit Herzinsuffizienz einhergehende ventrikuläre Arrhythmien (Torsades-de-Pointes) führen.
Diese Kombination darf nur unter engmaschiger klinischer Beobachtung und EKG-Überwachung insbesondere zu Beginn der Behandlung, verabreicht werden.
Kombinationen, die Vorsichtsmaβnahmen bei der Anwendung erfordern
Kardiovaskuläre Arzneimittel
Antiarrhythmika
- Propafenon weist negativ inotrope und betablockierende Eigenschaften auf, die additiv zu den Eigenschaften von Propranolol wirken können.
- Der Metabolismus von Propranolol ist bei gleichzeitiger Gabe von Chinidin vermindert, was zu einer zwei- bis dreifach erhöhten Blutkonzentration und einem grösseren Ausmass der klinischen Betablockade führt.
- Antiarrhythmika Klasse I (z.B. Disopyramid) und Amiodaron sind Antiarrhythmika mit negativ chronotropen Eigenschaften, die additiv zu den bei Betarezeptorenblockern wie Propranolol nachgewiesenen Eigenschaften wirken können. Durch Unterdrückung der sympathischen Kompensationsmechanismen kann zu Störungen der kardialen Kontraktilität und Erregungsleitung kommen.
- Die Metabolisierung von Lidocain wird durch die gleichzeitige Gabe von Propranolol gehemmt, was zu 25% höheren Lidocain-Konzentrationen führt. Nach gleichzeitiger Anwendung von Propranolol wurde über eine Lidocain-Toxizität (unerwünschte neurologische und Herzwirkungen) berichtet.
Digitalisglykoside
Digitalisglykoside und Betarezeptorenblocker verlängern beide die atrioventrikuläre Überleitungszeit und senken die Herzfrequenz. Die gleichzeitige Gabe kann das Bradykardierisiko erhöhen. Der Rat eines Kardiologen sollte eingeholt werden.
Dihydropyridine
Vorsicht ist geboten, wenn bei Patienten, die einen Betarezeptorenblocker erhalten, ein Dihydropyridin angewendet wird. Beide Wirkstoffe können Hypotonie und/ oder Herzinsuffizienz bei Patienten hervorrufen, deren Herzfunktion partiell durch additive inotrope Effekte kontrolliert wird. Die gleichzeitige Gabe kann die reflektorische Sympathikus-Reaktion, die bei überschiessender distaler Gefässerweiterung aktiviert ist, vermindern.
Blutdrucksenkende Mittel (ACE-Hemmer, Angiotensin-II-Rezeptoren-Antagonisten, Diuretika, Alpha-Blocker gleich welcher Indikation, zentral wirksame blutdrucksenkende Mittel, Reserpin, usw.)
In Kombination mit Betarezeptorenblockern können Blutdrucksenkende Arzneimittel Hypotonie, insbesondere orthostatische Hypotonie hervorrufen oder verstärken. Hinsichtlich zentral wirksamer blutdrucksenkender Mittel können Betarezeptorenblocker, die nach abruptem Absetzen von Clonidin möglicherweise auftretende Rebound-Hypertonie verstärken. Propranolol muss mehrere Tage vor Beendigung der Behandlung mit Clonidin abgesetzt werden.
Nicht kardiovaskuläre Arzneimittel
Kortikosteroide
Bei Patienten mit infantilem Hämangiom könnte ein erhöhtes Risiko bestehen, wenn sie eine Behandlung mit Kortikosteroiden erhalten haben oder derzeit begleitend erhalten, da die adrenale Suppression zu einem Verlust der gegenregulierenden Kortisolantwort führen und das Hypoglykämierisiko erhöhen kann. Dies gilt auch für gestillte Kinder, deren Mütter hochdosiert und langanhaltend mit Kortikosteroiden behandelt werden.
Orthostatische Hypotonie-induzierende Arzneimittel
Diese Arzneimittel können eine posturale Hypotonie induzieren (Nitratderivate, Phosphodiesterase-5-Hemmer, trizyklische Antidepressiva, Antipsychotika, Dopaminagonisten, Levopoda, Amifostin, Baclofen…), welche bei gleichzeitiger Gabe von Propranolol verstärkt werden kann. Der Rat eines Kardiologen sollte eingeholt werden.
Chlorpromazin
Bei gleichzeitiger Gabe von Propranolol und Chlorpromazin kann es zu erhöhten Plasmaspiegeln beider Substanzen kommen. Dies kann zu einem verstärkten antipsychotischen Effekt von Chlorpromazin und zu einer stärkeren antihypertensiven Wirkung von Propranolol führen.
Sympathomimetika
Die gleichzeitige Verabreichung von Sympathomimetika, z.B. Adrenalin, kann die Wirkung von Betablockern antagonisieren. Die parenterale Verabreichung von adrenalinhaltigen Medikamenten kann bei Patienten unter Betablockern in seltenen Fällen zu vasokonstriktion, Hypertonie und Bradykardie führen.
Ergotamin
Vorsicht ist geboten bei der gleichzeitigen Verabreichung von Propranolol und Ergotamin, Dihydroergotamin oder ähnliche Substanzen. Eine solche Kombination rief vereinzelt vasospastische Reaktionen hervor.
Hypoglykämische Wirkstoffe
Alle Betarezeptorenblocker können bestimmte Symptome einer Hypoglykämie maskieren: Herzklopfen und Tachykardie.
Bei der Anwendung von Propranolol neben einer hypoglykämischen Therapie bei Diabetespatienten ist Vorsicht geboten, da die hypoglykämische Reaktion auf Insulin verlängert sein könnte. In diesem Fall müssen die betreuenden Personen informiert und der Blutzuckerspiegel häufiger gemessen werden, insbesondere zu Beginn der Behandlung.
Lipidsenker
Bei gleichzeitiger Anwendung von Cholestyramin oder Colestipol und Propranolol waren die Propranolol-Konzentrationen um bis zu 50% erniedrigt.
Inhalationsnarkotika
Inhalationsnarkotika können sowohl die Kontraktionsfähigkeit des Herzmuskels als auch die kompensatorische Gefässkontraktion herabsetzen, wenn sie zusammen mit Propranolol verabreicht werden. Betastimulierende Wirkstoffe können verwendet werden, um die betablockierende Wirkung aufzuheben.
Substrate oder Inhibitoren von CYP2D6
Die Blutspiegel und/oder Toxizität von Propranolol können bei gleichzeitiger Gabe von Substraten oder Inhibitoren von CYP2D6,
wie Amiodaron, Cimetidin, Fluoxetin, Paroxetin, Chinidin und Ritonavir, erhöht sein. Mit Ranitidin oder Lansoprazol wurden keine Wechselwirkungen festgestellt.
Substrate oder Inhibitoren von CYP1A2
Die Blutspiegel und/oder Toxizität von Propranolol können bei gleichzeitiger Gabe von Substraten oder Inhibitoren von CYP1A2,
wie Amiodaron, Imipramin, Cimetidin, Ciprofloxacin, Fluvoxamin, Isoniazid, Theophyllin, Zileuton, Zolmitriptan und Rizatriptan, erhöht sein.
Rizatriptan
Die gleichzeitige Verabreichung von Rizatriptan und Propranolol kann eine Erhöhung der AUC und Cmax von Rizatriptan um ca. 70-80% verursachen. Die erhöhte Exposition von Rizatriptan wird vermutlich durch die Hemmung des First-Pass Metabolismus (Monoaminoxidase-A) von Rizatriptan verursacht. Falls beide Arzneimittel verordnet werden, wird für Rizatriptan eine Dosisanpassung empfohlen.
Substrate oder Inhibitoren der CYP2C19
Die Blutspiegel und/oder Toxizität von Propranolol können bei gleichzeitiger Gabe von Substraten oder Inhibitoren von CYP2C19,
wie Fluconazol, Cimetidin, Fluoxetin, Fluvoxamin, Teniposid und Tolbutamid, erhöht sein. Mit Omeprazol wurden keine Wechselwirkungen festgestellt.
Induktoren des Arzneimittelstoffwechsels
Bei gleichzeitiger Gabe von Induktoren wie Rifampicin, Ethanol, Phenytoin und Phenobarbital können die Blutspiegel von Propranolol erniedrigt sein.
Schwangerschaft/Stillzeit
Nicht relevant.
Stillende Frauen: siehe Abschnitt «Warnhinweise und Vorsichts-massnahmen» und Abschnitt „Interaktionen“
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Nicht relevant.
Unerwünschte Wirkungen
Zusammenfassung des Sicherheitsprofils
In klinischen Studien zum proliferativen infantilen Hämangiom wurden bei Säuglingen, die mit Hemangiol behandelt wurden, folgende unerwünschte Wirkungen am häufigsten berichtet: Schlafstörungen, Verschlechterung von Atemwegsinfektionen wie Bronchitis und Bronchiolitis in Verbindung mit Husten und Fieber sowie Durchfall und Erbrechen.
Sicherheit von Hemangiol wurde nicht bei Patienten im Alter >1Jahr untersucht.
Im Allgemeinen waren die unerwünschten Wirkungen, über die im Rahmen eines Sonderbewilligung-Programms und in der Literatur berichtet wurde, Hypoglykämie (und damit im Zusammenhang stehende Ereignisse wie hypoglykämische Krampfanfälle) sowie Verschlechterung von Atemwegsinfektionen mit Atemnot.
In der folgenden Tabelle sind die unerwünschten Wirkungen aufgeführt, bei denen ein Zusammenhang zum Arzneimittel vermutet wurde und die, unabhängig von der Dosis und Behandlungsdauer, im Rahmen zweier klinischer Studien mit 424 Patienten berichtet wurden. Die Patienten wurden mit Hemangiol in Dosen von 1 oder 3 mg/kg/Tag maximal 6 Monate lang behandelt.
Die Häufigkeit dieser unerwünschten Wirkungen ist wie folgt definiert: sehr häufig (≥1/10), häufig (≥1/100 bis < 1/10), gelegentlich (≥1/1'000 bis < 1/100), selten (≥1/10'000 bis < 1/1'000), sehr selten (< 1/10'000), nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar). Aufgrund der Grösse der klinischen Datenbank sind die Kategorien «selten» und «sehr selten» nicht vertreten.
Innerhalb jeder Systemorganklasse sind die Nebenwirkungen nach abnehmendem Schweregrad angegeben.
System Organklasse | Sehr häufig | Häufig | Gelegentlich | Nicht bekannt |
|---|---|---|---|---|
Infektionen und parasitäre Erkrankungen | Bronchitis | Bronchiolitis | ||
Stoffwechsel und Ernährungsstörungen | Verminderter Appetit | |||
Psychiatrische Erkrankungen | Schlafstörungen | Agitation Reizbarkeit | ||
Erkrankungen des Nervensystems | Somnolenz | Hypo-glykämischer Krampfanfall | ||
Herzerkrankungen | AV-Block | Bradykardie | ||
Gefäss Erkrankungen | Periphere Kälte | Hypotonie, Vasokontrik-tion, Raynaud-Syndrom | ||
Erkrankungen der Atemwege, des Brustraums und des Media-stinums | Broncho-spasmus | |||
Erkrankungen des Gastrointestinal-trakts | Durchfall, Erbrechen | Verstopfung, Bauchschmerzen | ||
Erkrankungen der Haut und des Unterhautzell-gewebes | Erythem Windel-dermatitis | Urtikaria, Haarausfall | Psoriasiforme Dermatitis | |
Untersuchungen | Verminderter Blutdruck | Verminderter Blutzucker, Verlangsamte Herzfrequenz | Agranulo-zytose, Hyper-kaliämie |
Beschreibung ausgewählter unerwünschter Wirkungen
Bezüglich der Infektionen der unteren Atemwege wie Bronchitis oder Bronchiolitis wurde bei Patienten, die mit Hemangiol behandelt wurden, aufgrund der bronchokonstriktiven Wirkung von Propranolol eine Verschlechterung der Symptome (einschliesslich Broncho-spasmus) beobachtet. Diese Wirkungen führten in seltenen Fällen zu einem endgültigen Absetzen der Behandlung (siehe Abschnitt Warnhinweise und Vorsichtsmassnahmen).
Bei den Schlafstörungen handelte es sich um Schlaflosigkeit, schlechte Schlafqualität und Hypersomnie. Sonstige Zentralnerven-system-Störungen wurden hauptsächlich in den frühen Phasen der Behandlung beobachtet.
Häufig wurde über Durchfall berichtet, der nicht immer mit einer infektiösen Erkrankung des Gastrointestinaltraktes einherging. Das Auftreten von Durchfall scheint zwischen 1 und 3 mg/kg/Tag dosisabhängig zu sein. Keiner der Fälle war schwerwiegend oder führte zum Behandlungsabbruch.
Die während klinischer Studien berichteten kardiovaskulären Ereignisse verliefen asymptomatisch. Im Rahmen der 4-stündigen Überwachung der Herz-Kreislauf-Funktion während der Titrationstage wurde nach Verabreichung des Arzneimittels ein Rückgang von Herzfrequenz (etwa 7 bpm) und systolischem Blutdruck (weniger als 3 mmHg) beobachtet. In einem Fall führte ein atrioventrikulärer Herzblock 2. Grades bei einem Patienten mit zugrundeliegender Überleitungsstörung zu einem endgültigen Abbruch der Behandlung. In der Literatur wird über Einzelfälle von symptomatischer Bradykardie und Hypotonie berichtet.
Die während klinischer Studien beobachteten Blutzuckersenkungen waren asymptomatisch. Im Rahmen des Sonderbewilligung-Programms und in der Literatur wurde jedoch mehrfach über Hypoglykämie mit einem damit im Zusammenhang stehenden hypoglykämischen Krampfanfall berichtet, insbesondere bei Nahrungskarenz während einer interkurrenten Erkrankung (siehe Abschnitt Warnhinweise und Vorsichtsmassnahmen).
Die gleichzeitige Behandlung mit systemischen Kortikosteroiden kann das Hypoglykämierisiko erhöhen (siehe Abschnitt Warnhinweise und Vorsichtsmassnahmen).
In der Literatur wurde von einigen wenigen Hyperkaliämie Fällen bei Patienten mit groβen ulzerierten Hämangiomen berichtet (siehe Abschnitt Warnhinweise und Vorsichtsmassnahmen).
Fertilität
In der Literatur wurde von einigen, reversiblen, Wirkungen auf die männliche und weibliche Fertilität in erwachsenen Ratten berichtet. Eine Studie in juvenilen Ratten zeigte jedoch keinen Effekt auf die Fertilität.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen ist wichtig, um weitere Informationen zur kontinuirlichen Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels zusammenzutragen.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
Überdosierung
Bei der Toxizität von Betarezeptorenblockern handelt es sich um eine Ausdehnung ihrer therapeutischen Wirkungen:
- Herzsymptome einer leichten bis mittelschweren Intoxikation sind verminderte Herzfrequenz und Hypotonie. Bei stärkerer Intoxikation können atrioventrikulärer Block, intraventrikuläre Überleitungsverzögerungen und kongestive Herzinsuffizienz auftreten.
- Insbesondere bei Asthma-Patienten kann ein Bronchospasmus auftreten.
- Es kann zu einer Hypoglykämie kommen, deren Manifestationen (Tremor, Tachykardie) durch die anderen klinischen Wirkungen der Beta-Blocker-Toxizität maskiert werden.
Propranolol ist stark fettlöslich und kann die Blut-Hirn-Schranke überwinden und Krampfanfälle hervorrufen.
Unterstützende Massnahmen und Behandlung:
Der Patient sollte an einen Herzmonitor angeschlossen und Vitalparameter, geistiger Zustand und Blutzucker überwacht werden. Intravenöse Flüssigkeitszufuhr bei Hypotonie und Gabe von Atropin bei Bradykardie sollte erfolgen. Spricht der Patient nicht ausreichend auf die intravenöse Flüssigkeitszufuhr an, sind Glukagon und anschliessend Katecholamine zu erwägen. Bei einem Bronchospasmus können Isoproterenol und Aminophyllin angewendet werden.
Eigenschaften/Wirkungen
ATC-Code
C07AA05
Wirkungsmechanismus
In der Literatur beschriebene mögliche Wirkmechanismen von Propranolol beim proliferativen infantilen Hämangiom könnten mehrere, in engem Zusammenhang stehende Mechanismen umfassen:
- Eine lokale hämodynamische Wirkung (Vasokonstriktion als klassische Folge der beta-adrenergen Blockade und dadurch eine verminderte Durchblutung des infantilen Hämangioms);
- Eine antiangiogenetische Wirkung von Propranolol, gekennzeichnet durch eine Abnahme der Proliferation von vaskulären Endothelzellen, eine Reduktion der Neovaskularisation und der Bildung von Gefäβröhren sowie eine verminderte Sekretion von Matrix-Metalloproteinase 9;
- Eine apoptoseauslösende Wirkung auf die Kapillarendothelzellen;
Reduktion der VEGF- und bFGF-Signalwege und daraus resultierende Angiogenese/Proliferation.
Pharmakodynamik
Bei Propranolol handelt es sich um einen Betarezeptorenblocker, der durch drei pharmakologische Eigenschaften gekennzeichnet ist:
- Fehlen einer kardioselektiven Beta-1-betablockierenden Wirkung
- Antiarrhythmische Wirkung
Mangelnde partielle agonistische Aktivität (oder intrinsische sympathomimetische Aktivität).
Klinische Wirksamkeit
Die Wirksamkeit von Propranolol bei Säuglingen (Alter bei Behandlungsbeginn 5 Wochen bis 5 Monate) mit proliferativem infantilem Hämangiom, das einer systemischen Therapie bedarf, wurde im Rahmen einer zulassungsrelevanten randomisierten, kontrollierten, multizentrischen, adaptiven Mehrfachdosisstudie der Phase II/III untersucht, deren Ziel es war, vier Behandlungs-schemata von Propranolol (1 oder 3 mg/kg/Tag über 3 oder 6 Monate) mit Placebo zu vergleichen (doppelblind).
Die Behandlung wurde 456 Patienten verabreicht (401 erhielten Propranolol in einer Dosis von 1 oder 3 mg/kg/Tag über 3 oder 6 Monate, 55 erhielten Placebo), einschliesslich einer Aufdosierung von 3 Wochen. Die Patienten (71,3% weiblich; 37% im Alter von 35‑90 Tagen und 63% im Alter von 91‑150 Tagen) wiesen zu 70% ein Zielhämangiom am Kopf auf und die Mehrzahl der infantilen Hämangiome war örtlich begrenzt (89%).
Der Behandlungserfolg war als vollständiges oder nahezu vollständiges Abklingen des Zielhämangioms definiert, was durch verblindete zentralisierte unabhängige Bewertungen anhand von Fotografien aus Woche 24 ermittelt wurde, sofern die Behandlung nicht vorzeitig abgebrochen wurde.
Das Schema mit 3 mg/kg/Tag über 6 Monate, das am Ende des Phase-II-Teils der Studie ausgewählt wurde, führte bei 60,4% der Patienten zu einem Behandlungserfolg im Vergleich zu 3,6% im Placeboarm (p-Wert < 0,0001). In den nach Alter (35‑90 Tage/91‑150 Tage), Geschlecht und Ort des Hämangioms (Kopf/Körper) eingeteilten Untergruppen wurden keine Unterschiede hinsichtlich des Ansprechens auf Propranolol festgestellt. Bei 88% der Patienten wurde nach 5-wöchiger Behandlung mit Propranolol eine Verbesserung des Hämangioms beobachtet. Bei 11,4% der Patienten war nach Behandlungsende eine erneute Behandlung notwendig.
Aus ethischen Gründen in Bezug auf die Verwendung von Placebo wurde die Wirksamkeit in Patienten mit Hochrisiko-Hämangiomen nicht untersucht. Belege für die Wirksamkeit von Propranolol in Patienten mit Hochrisiko-Hämangiome sind der Literatur zu entnehmen sowie einem speziellen Sonderbewilligung-Programms, das mit Hemangiol durchgeführt wurde.
Ausgehend von einer retrospektiven Analyse benötigte eine Minderheit der Patienten (12%) eine erneute systemische Behandlung. Nach erneutem Beginn der Behandlung wurde bei der überwiegenden Mehrheit der Patienten ein zufriedenstellendes Ansprechen festgestellt.
Pharmakokinetik
Absorption
Nach oraler Applikation wird Propranolol nahezu vollständig resorbiert. Es unterliegt jedoch einem ausgedehnten First-Pass-Metabolismus durch die Leber und im Durchschnitt gelangen nur etwa 25% des Propranolols in den systemischen Kreislauf. Spitzenplasmakonzentrationen treten ungefähr 1 bis 4 Stunden nach einer oralen Dosis auf. Die Gabe von proteinreichen Nahrungsmitteln erhöht die Bioverfügbarkeit von Propranolol um etwa 50%, ohne dass sich die Zeit bis zum Erreichen der Spitzenkonzentration ändert.
Propranolol ist ein Substrat für den intestinalen Effluxtransporter P-Glykoprotein (P-gp). Studien legen jedoch nahe, dass P-gp für die intestinale Resorption von Propranolol im üblichen therapeutischen Dosisbereich nicht dosislimitierend ist.
Distribution
Ungefähr 90% des im Blut befindlichen Propranolols sind an Plasmaproteine (Albumin und saures Alpha-1-Glykoprotein) gebunden. Das Verteilungsvolumen von Propranolol beträgt ca. 4 l/kg. Propranolol überwindet die Blut-Hirn-Schranke sowie die Plazenta und geht in die Muttermilch über.
Metabolismus
Propranolol wird auf drei Hauptwegen metabolisiert: aromatische Hydroxylierung (hauptsächlich 4-Hydroxylierung), N-Dealkylierung gefolgt von weiterer Seitenkettenoxidation und direkte Glucuronidierung. Die prozentualen Beiträge dieser Wege zum Gesamtmetabolismus sind 42%, 41% bzw. 17%, allerdings gibt es eine beträchtliche Variabilität zwischen einzelnen Personen. Die vier wichtigsten Endmetaboliten sind Propranolol-Glucuronid, Naphthyloxy-Milchsäure und ‑Glucuronsäure sowie konjugierte Sulfate von 4-Hydroxy-Propranolol. In-vitro-Studien deuten darauf hin, dass CYP2D6 (aromatische Hydroxylierung), CYP1A2 (Kettenoxidation) und in einem geringeren Ausmass auch CYP2C19 an der Metabolisierung von Propranolol beteiligt sind. 4-Hydroxy-Propranolol ist ein schwacher Inhibitor von CYP2D6.
Elimination
Hinsichtlich der renalen Clearance oder der Eliminationshalbwertszeit wurde bei gesunden Probanden kein Unterschied zwischen extensiven und schwachen CYP2D6-Metabolisierern festgestellt.
Die Plasmahalbwertszeit von Propranolol liegt im Bereich von 3 bis 6 Stunden. Weniger als 1% der Dosis wird als unveränderte Substanz im Urin ausgeschieden.
Kinetik spezieller Patientengruppen
Kinder und Jugendliche
Die Pharmakokinetik von Hemangiol wurde bei 19 Säuglingen im Alter von 35 bis 150 Tagen untersucht. Nach Gabe von 3 mg/kg/Tag verteilt auf 2 Einnahmen wurden im Steady-State maximale Plasmakonzentration im Allgemeinen 2 Stunden nach Applikation gemessen.
Der entsprechende Mittelwert lag unabhängig vom Alter des Säuglings bei ungefähr 79 ng/ml.
Die scheinbare renale Clearance betrug 2,71 l/h/kg bei Säuglingen im Alter von 65‑120 Tagen und 3,27 l/h/kg bei 181‑240 Tage alten Säuglingen. Um das Körpergewicht korrigiert, waren die bei Säuglingen festgestellten primären pharmakokinetischen Parameter für Propranolol (wie Plasma-Clearance) ähnlich den in der Literatur berichteten Parametern für Erwachsene.
Der Metabolit 4-Hydroxy-Propranolol wurde quantifiziert; seine Plasmaexposition war im Vergleich zur Exposition gegenüber der Muttersubstanz weniger als 7%.
Präklinische Daten
Als Hauptwirkungen nach wiederholter Gabe von Propranolol wurden bei adulten und juvenilen Ratten über eine vorübergehende Verringerung des Körpergewichts berichtet.
In-vitro- und In-vivo-Daten lassen den Schluss zu, dass Propranolol kein genotoxisches Potenzial besitzt.
In Studien, in denen Mäuse und Ratten Propranololhydrochlorid bis zu 18 Monate lang in Dosen von bis zu 150 mg/kg/Tag über die Nahrung erhielten, gab es keine Hinweise auf Karzinogenität.
In adulten weiblichen Ratten verhinderte in den Uterus oder intravaginal verabreichtes Propranolol bei einer Dosis von ≥4 mg pro Tier die Implantation. Bei adulten männlichen Ratten induzierte die wiederholte Verabreichung von Propranolol in hohen Dosen (≥7,5 mg/kg) histopathologische Läsionen der Hoden, der Nebenhoden und der Samenstränge, eine Abnahme der Beweglichkeit der Spermien, der Spermienzellkonzentration und des Plasmatestosteronspiegels sowie einen erheblichen Anstieg von Spermienanomalien. Im Allgemeinen waren diese Wirkungen nach der Einstellung der Behandlung reversibel. Ähnliche Ergebnisse wurden nach einer intra-testikulären Verabreichung von Propranolol und in in vitro-Modellen erhalten.
Die potenziellen Wirkungen von Propranolol auf die Entwicklung juveniler Ratten wurden nach täglicher oraler Gabe ab Tag 4 bis Tag 21 nach der Geburt in Dosisstufen von 0, 10, 20 oder 40 mg/kg/Tag beurteilt.
Mortalität sowie eine reversible verminderte Gewichtszunahme wurden mit 40 mg/kg/Tag festgestellt. Dies führte zu einem NOAEL von 20 mg/kg/Tag für juvenile Toxizität.
Hinsichtlich des Wachstums, der körperlichen und neurologischen Entwicklung und der Fortpflanzungsfähigkeit wurden bis zur höchsten Dosis keine auf Propranolol zurückzuführenden Effekte festgestellt. Dies entspricht einem Sicherheitsabstand von 1,2 in weiblichen und 2,9 in männlichen Patienten basierend auf durchschnittlichen Expositionswerten am Tag 21.
Sonstige Hinweise
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Haltbarkeit nach Anbruch: 2 Monate
Die Flasche vor Gebrauch nicht schütteln.
Besondere Lagerungshinweise
Hemangiol ist gut verschlossen in der Originalverpackung und für Kinder unerreichbar bei Raumtemperatur (15-25°C) und vor Licht geschützt aufzubewahren. Das Präparat darf nicht eingefroren werden.
Der Flasche liegt eine Oralspritze graduiert in mg Propranolol Base bei.
Zulassungsnummer
61214 (Swissmedic).
Zulassungsinhaberin
Pierre Fabre (Suisse) S.A., Allschwil.
Stand der Information
September 2020.
Composition
Principes actifs
Propranolol sous forme de chlorhydrate de propranolol.
Excipients
Arôme vanille et arôme fraise (contenant 2,6 mg/ml de propylène-glycol), saccharine sodique (contenant 0,17 mg/ml de sodium), hydroxyéthylcellulose (produite à base de coton génétiquement modifié), acide citrique monohydraté, eau purifiée.
Forme pharmaceutique et quantité de principe actif par unité
1 ml de solution buvable contient 3,75 mg de propranolol base sous forme de 4,28 mg de chlorhydrate de propranolol.
Indications/Possibilités d’emploi
Hemangiol est indiqué dans le traitement des hémangiomes infantiles prolifératifs nécessitant un traitement systémique:
Le traitement doit être instauré chez les enfants âgés de 5 semaines à 5 mois.
Posologie/Mode d’emploi
Le traitement doit être instauré par un médecin expérimenté dans le diagnostic, le traitement et la prise en charge des hémangiomes infantiles, dans un environnement clinique contrôlé dans lequel des installations adéquates pour la prise en charge des réactions indésirables, y compris celles nécessitant des mesures d'urgence, sont disponibles.
Posologie
La posologie est exprimée en propranolol base.
La dose initiale recommandée est de 1 mg/kg/jour, répartie en deux prises séparées de 0,5 mg/kg. Si le patient supporte bien le médicament, la dose peut être augmentée, seulement sous surveillance médicale, de la manière suivante: 1 mg/kg/jour pendant 1 semaine, puis 2 mg/kg/jour pendant 1 semaine, puis 3 mg/kg/jour en dose d'entretien.
La dose thérapeutique est de 3 mg/kg/jour, administrée en 2 prises séparées de 1,5 mg/kg, le matin et en fin d'après-midi, avec un intervalle d'au moins 9 heures entre deux prises. Le médicament doit être pris pendant ou juste après un repas.
Hemangiol doit être administré pendant ou juste après un repas afin d'éviter le risque d'hypoglycémie. Si l'enfant ne mange pas ou vomit, il est recommandé de ne pas administrer la dose.
Si l'enfant recrache une dose ou ne prend pas tout le médicament, il convient de ne pas lui administrer une autre dose et d'attendre la dose suivante prévue.
Au cours de la phase de titration, chaque augmentation posologique doit être réalisée sous surveillance médicale dans les mêmes conditions que pour l'administration de la dose initiale. Après la phase de titration, la dose sera réajustée par le médecin en fonction de l'évolution du poids de l'enfant (voir le tableau 1).
Tableau 1. Dose en fonction du poids
Semaine 1 | Semaine 2 | Semaine 3 (dose d'entretien) | |
Poids (kg) | Dose administrée deux fois par jour | ||
2 à <2.5 | 1 mg | 2 mg | 3 mg |
2.5 à <3 | 1 mg | 2.5 mg | 3.5 mg |
3 à <3.5 | 1.5 mg | 3 mg | 4.5 mg |
3.5 à <4 | 1.5 mg | 3.5 mg | 5 mg |
4 à <4.5 | 2 mg | 4 mg | 6 mg |
4.5 à <5 | 2 mg | 4.5 mg | 6.5 mg |
5 à <5.5 | 2.5 mg | 5 mg | 7.5 mg |
5.5 à <6 | 2.5 mg | 5.5 mg | 8 mg |
6 à <6.5 | 3 mg | 6 mg | 9 mg |
6.5 à <7 | 3 mg | 6.5 mg | 9.5 mg |
7 à <7.5 | 3.5 mg | 7 mg | 10.5 mg |
7.5 à <8 | 3.5 mg | 7.5 mg | 11 mg |
8 à <8.5 | 4 mg | 8 mg | 12 mg |
8.5 à <9 | 4 mg | 8.5 mg | 12.5 mg |
9 à <9.5 | 4.5 mg | 9 mg | 13.5 mg |
9.5 à <10 | 4.5 mg | 9.5 mg | 14 mg |
10 à <10.5 | 5 mg | 10 mg | 15 mg |
10.5 à <11 | 5 mg | 10.5 mg | 15.5 mg |
11 à <11.5 | 5.5 mg | 11 mg | 16.5 mg |
11.5 à <12 | 5.5 mg | 11.5 mg | 17 mg |
12 à <12.5 | 6 mg | 12 mg | 18 mg |
Une surveillance clinique de l'état de l'enfant et un réajustement de la posologie doivent être effectués au moins une fois par mois.
Durée du traitement
Hemangiol doit être administré pendant une période de 6 mois.
L'arrêt du traitement ne nécessite pas de diminution progressive de la dose.
Chez la minorité de patients qui présentent une rechute des symptômes après l'arrêt du traitement, celui-ci peut être réintroduit dans les mêmes conditions.
Populations particulières
En l'absence de données d'efficacité clinique et de sécurité, Hemangiol ne doit pas être utilisé chez l'enfant âgé de moins de 5 semaines. En l'absence de données d'efficacité clinique et de sécurité dans les essais cliniques menés avec Hemangiol, l'instauration d'un traitement par Hemangiol chez l'enfants en bas âge et l'enfant âgé de plus de 5 mois n'est pas recommandée.
Patients présentant des troubles de la fonction hépatique ou de la fonction rénale
En l'absence de données, l'administration du produit n'est pas recommandée chez l'enfant insuffisant hépatique ou rénal.
Mode d'administration
Hemangiol doit être administré directement dans la bouche de l'enfant à l'aide de la seringue pour administration orale graduée en mg de propranolol base fournie avec le flacon de solution buvable.
Le flacon ne doit pas être agité avant utilisation.
Si nécessaire, le médicament peut être dilué dans une petite quantité de lait pour bébé ou de jus de pomme et/ou d'orange adapté à l'âge de l'enfant. Ne pas verser le produit dans un biberon plein.
Le mélange peut être effectué avec une cuillerée à café (environ 5 ml) de lait pour les enfants pesant jusqu'à 5 kg ou avec une cuillerée à soupe (environ 15 ml) de lait ou de jus de fruits pour les enfants pesant plus de 5 kg et administré dans un biberon. Le mélange doit être utilisé dans un délai de 2 heures.
Hemangiol et le repas doivent être donnés par la même personne afin d'éviter le risque d'hypoglycémie. Si plusieurs personnes sont impliquées, une bonne communication est essentielle pour garantir la sécurité de l'enfant.
Contre-indications
- Prématuré n'ayant pas atteint l'âge corrigé de 5 semaines (l'âge corrigé étant calculé en soustrayant le nombre de semaines de prématurité de l'âge réel)
- Poids <2kg
- Enfant allaité par sa mère traitée par des médicaments contre-indiqués avec le propranolol
- Hypersensibilité à la substance active ou à l'un des excipients
- Asthme ou antécédent de bronchospasme
- Blocs auriculo-ventriculaires de second ou troisième degré
- Maladie du sinus (y compris bloc sino-auriculaire)
- Bradycardie au-dessous des limites suivantes:
Age | 0-3 mois | 3-6 mois | 6-12 mois |
Fréquence cardiaque (battements/min) | 100 | 90 | 80 |
- Hypotension artérielle au-dessous des limites suivantes:
Age | 0-3 mois | 3-6 mois | 6-12 mois |
Pression artérielle (mm Hg) | 65/45 | 70/50 | 80/55 |
- Choc cardiogénique
- Insuffisance cardiaque non contrôlée par un traitement
- Angor de Prinzmetal
- Troubles artériels périphériques sévères (syndrome de Raynaud)
- Enfants prédisposés à l'hypoglycémie
- Phéochromocytome
Mises en garde et précautions
Mise sous traitement
Avant la mise sous traitement par propranolol, un dépistage des risques associés à l'utilisation de propranolol doit être réalisé. Une analyse des antécédents médicaux et un examen clinique complet doivent être effectués, incluant la mesure de la fréquence cardiaque ainsi qu'une auscultation cardiaque et pulmonaire.
En cas de suspicion d'anomalie cardiaque, il convient de consulter un spécialiste avant la mise sous traitement afin de rechercher une éventuelle contre-indication sous-jacente.
En cas d'anomalie broncho-pulmonaire aiguë, la mise sous traitement doit être différée.
Hypoglycémie
Le propranolol s'oppose à la réponse des catécholamines endogènes permettant de corriger une hypoglycémie. Il masque les signes adrénergiques annonciateurs d'hypoglycémie, en particulier tachycardie, tremblements, anxiété et faim. Il peut aggraver les hypoglycémies survenant chez l'enfant, en particulier en cas de jeûne (p.ex. absence de prise de nourriture, infections, vomissements), en cas de besoins accrus en glucose (refroidissement, stress, infections) ou en cas de surdosage.
Ces hypoglycémies associées à la prise de propranolol peuvent se présenter exceptionnellement sous forme de crise convulsive et/ou de coma.
En cas d'apparition de signes cliniques d'hypoglycémie, il est nécessaire de faire boire à l'enfant une solution liquide sucrée et d'interrompre temporairement le traitement. Une surveillance appropriée de l'enfant sera mise en place jusqu'à disparition des symptômes.
Le médecin prescripteur doit informer les soignants/parents du risque d'hypoglycémie sévère, qui reste important pendant toute la durée du traitement, et insister sur la nécessité de respecter les recommandations posologiques (voir rubrique Posologie/mode d'emploi).
Les soignants doivent être instruits des signes cliniques permettant d'identifier une hypoglycémie afin
- de traiter immédiatement un épisode hypoglycémique et d'éviter des situations menaçant le pronostic vital,
- de contacter un médecin ou d'aller directement à l'hôpital,
- d'arrêter le traitement.
Chez l'enfant diabétique, la glycémie doit être surveillée plus fréquemment et contrôlée par un endocrinologue.
L'administration concomitante du propranolol avec les corticoïdes peut augmenter le risque d'hypoglycémie.
Affections respiratoires
En cas d'infection des voies respiratoires inférieures associée à une dyspnée avec sibilants, le traitement doit être temporairement interrompu. L'administration de bêta-2 agonistes et de corticoïdes inhalés est possible. La reprise du propranolol peut être envisagée, sous surveillance médicale, après que l'enfant a complètement récupéré; en cas de récidive, le traitement doit être définitivement arrêté.
En cas de bronchospasme isolé, le traitement doit être définitivement arrêté.
Affections cardiovasculaires
Le propranolol, de par son action pharmacologique, peut entraîner ou majorer une bradycardie ou des troubles de la pression artérielle. On diagnostiquera une bradycardie si la fréquence cardiaque diminue de plus de 30 bpm par rapport à la fréquence initiale. La bradycardie est définie comme une fréquence cardiaque inférieure aux limites suivantes:
Age | 0-3 mois | 3-6 mois | 6-12 mois |
Fréquence cardiaque (battements/min) | 100 | 90 | 80 |
Après la mise sous traitement et après toute augmentation de dose, une surveillance clinique, incluant la pression artérielle et la fréquence cardiaque, doit être effectuée pendant au moins 4 heures. En cas de bradycardie symptomatique ou de bradycardie inférieure à 80 bpm, il convient de consulter immédiatement un spécialiste.
En cas de bradycardie sévère et/ou symptomatique ou d'hypotension artérielle survenant à n'importe quel moment au cours du traitement, il convient d'interrompre le traitement et de consulter un spécialiste.
Insuffisance cardiaque
La stimulation sympathique peut être un élément vital pour soutenir la fonction circulatoire en cas d'insuffisance cardiaque congestive et son inhibition par bêta-blocage peut aggraver la défaillance. Chez l'enfant insuffisant cardiaque, le traitement doit être pris en charge par un cardiologue.
Syndrome PHACE
Les données de sécurité concernant l'utilisation du propranolol chez les patients atteints de syndrome PHACE sont très limitées.
Le propranolol peut accroître le risque d'accident vasculaire cérébral chez les patients atteints de syndrome PHACE avec des anomalies cérébrovasculaires sévères en réduisant la pression artérielle et en diminuant le débit sanguin dans les vaisseaux occlus, rétrécis ou sténosés.
Les enfants qui présentent un hémangiome infantile facial étendu doivent faire l'objet d'investigations approfondies pour rechercher une éventuelle artériopathie associée à un syndrome PHACE, par angiographie par résonance magnétique de la tête et du cou et par imagerie cardiaque pour visualiser la crosse aortique, avant d'envisager un traitement par le propranolol.
Il convient de consulter un spécialiste.
Allaitement
Le propranolol passe dans le lait maternel, les mères traitées par le propranolol qui allaitent leur enfant doivent en informer leur médecin.
Insuffisance hépatique ou rénale
Le propranolol est métabolisé au niveau hépatique et éliminé par le rein. En l'absence de données chez l'enfant, le propranolol n'est pas recommandé en cas d'insuffisance rénale ou hépatique.
Hypersensibilité
Chez les patients susceptibles de faire une réaction anaphylactique sévère, quelle qu'en soit l'origine, en particulier avec des produits de contraste iodés, le traitement par bêtabloquant peut entraîner une aggravation de la réaction et une résistance au traitement par adrénaline aux posologies habituelles. Un risque accru d'anaphylaxie doit être pris en compte lors de l'évaluation du rapport bénéfice/risque de l'utilisation d'Hemangiol.
Hemangiol contient moins de 1 mmol (23 mg) de sodium par flacon, c'est-à-dire qu'il est presque «sans sodium».
La dose maximale journalière d'Hemangiol contient 2,08 mg de propylène-glycol/kg/jour.
L'administration concomitante d'un substrat de l'alcool déshydrogénase, tel que l'éthanol, peut induire des effets indésirables graves chez le nouveau-né.
Anesthésie générale
Les bêtabloquants entraînent une atténuation de la tachycardie réflexe et une augmentation du risque d'hypotension. Il convient de prévenir l'anesthésiste que le patient est traité par un bêtabloquant et c'est à lui/elle de décider dans quel cas et pour combien de temps le traitement doit être interrompu avant l'intervention.
Hyperkaliémie
Des cas d'hyperkaliémie ont été rapportés chez des patients avec des hémangiomes ulcérés étendus. Une surveillance des électrolytes doit être réalisée chez ces patients.
Psoriasis
Chez les patients souffrant de psoriasis, des aggravations de la maladie ayant été rapportées sous bêtabloquants; l'indication mérite d'être pesée.
Interactions
En l'absence d'études spécifiques chez l'enfant, les interactions médicamenteuses avec le propranolol sont celles déjà connues chez l'adulte. Avant d'administrer d'autres médicaments, il convient de tenir compte des 2 situations suivantes (non mutuellement exclusives):
- Enfant recevant tout autre médicament, notamment parmi ceux mentionnés ci-dessous.
- Enfant allaité par sa mère prenant tout autre médicament, notamment parmi ceux mentionnés ci-dessous. Dans ce cas, la nécessité d'arrêter l'allaitement doit être discutée.
Une surveillance clinique étroite à la recherche d'une éventuelle intolérance au propranolol est nécessaire.
Effet du propranolol sur les médicaments co-administrés:
L'effet du propranolol sur la concentration plasmatique des médicaments co-administrés est présenté dans le tableau ci-dessous:
Médicament co-administré avec le propranolol | Effet sur la concentration plasmatique des médicaments co-administrés |
Anesthésiques locaux de type amide (lidocaïne, bupivacaïne, mépivacaïne) | Augmentation |
Warfarine | Augmentation |
Propafénone | Augmentation >200% |
Nifédipine | Augmentation 80% |
Vérapamil | Inchangé |
Pravastatine, lovastatine | Diminution 20% |
Fluvastatine | Inchangé |
Zolmitriptan | Augmentation 60% |
Rizatriptan | Augmentation 80% |
Thioridazine | Augmentation 370% |
Diazépam | Augmentation |
Oxazépam, triazolam, lorazépam, alprazolam | Inchangé |
Théophylline | Augmentation 70% |
Effet des médicaments co-administrés sur le propranolol:
L'effet des médicaments co-administrés sur la concentration plasmatique du propranolol est présenté dans le tableau ci-dessous:
Médicament co-administré avec le propranolol | Effet sur la concentration plasmatique du propranolol |
Inhibiteurs de CYP2D6, CYP1A2 ou CYP2C19 | Augmentation |
Inducteurs de CYP1A2 ou CYP2C19 | Diminution |
Quinidine | Augmentation >200% |
Nisoldipine | Augmentation 50% |
Nicardipine | Augmentation 80% |
Chlorpromazine | Augmentation 70% |
Cimétidine | Augmentation 50% |
Cholestyramine, colestipol | Augmentation 50% |
Alcool | Augmentation (aigüe), diminution (chronique) |
Diazépam | Inchangé |
Vérapamil | Inchangé |
Métoclopramide | Inchangé |
Ranitidine | Inchangé |
Lansoprazole | Inchangé |
Oméprazole | Inchangé |
Propafénone | Augmentation 200% |
Hydroxyde d'aluminium | Augmentation 50% |
Associations déconseillées
Inhibiteurs calciques bradycardisants (diltiazem, vérapamil, bépridil)
L'administration concomitante avec le propranolol peut entraîner des troubles de l'automatisme (bradycardie excessive, arrêt sinusal), des troubles de la conduction sino-auriculaire et auriculoventriculaire et un risque majoré de troubles du rythme ventriculaire (torsades de pointes) ainsi qu'une insuffisance cardiaque.
Une telle association ne doit se faire que sous surveillance clinique et ECG étroite, notamment en début de traitement.
Associations nécessitant des précautions d'emploi lors de l'administration
Médicaments cardiovasculaires
Antiarythmiques
- La propafénone a des propriétés inotropes négatives et bêtabloquantes qui peuvent s'ajouter à celles du propranolol.
- Le métabolisme du propranolol est réduit par l'administration concomitante de quinidine, entraînant une augmentation de 2 à 3 fois de la concentration sanguine et des degrés plus importants de blocage bêta-adrénergique.
- Les antiarythmiques de classe I (par exemple disopyramide) et l'amiodarone sont des antiarythmiques dotés de propriétés chronotropes négatives qui peuvent s'ajouter à celles observées avec les bêtabloquants tels que le propranolol. Des troubles de l'automatisme et de la conduction sont prévisibles en raison de la suppression des mécanismes sympathiques compensateurs.
- Le métabolisme de la lidocaïne est inhibé par l'administration concomitante de propranolol, entraînant une augmentation de 25% des concentrations de lidocaïne. Une toxicité de la lidocaïne (événements indésirables neurologiques et cardiaques) a été rapportée après administration concomitante avec le propranolol.
Digitaliques
Les digitaliques ainsi que les bêtabloquants ralentissent la conduction auriculoventriculaire et diminuent la fréquence cardiaque. Leur utilisation concomitante peut majorer le risque de bradycardie. Il convient de demander conseil à un cardiologue.
Dihydropyridines
Il convient d'être prudent chez les patients sous bêtabloquant qui reçoivent une dihydropyridine. Les deux agents peuvent induire une hypotension artérielle et/ou une insuffisance cardiaque chez les patients dont la fonction cardiaque est partiellement contrôlée en raison de leurs effets inotropes additifs. Leur utilisation concomitante peut réduire la réponse sympathique réflexe en cas de vasodilatation distale excessive.
Antihypertenseurs (Inhibiteurs de l'Enzyme de Conversion (IEC), antagonistes des récepteurs de l'angiotensine II, diurétiques, alpha-bloquants quelle que soit l'indication, antihypertenseurs d'action centrale, réserpine, etc.)
Lorsqu'ils sont associés à des bêtabloquants, les médicaments qui diminuent la pression artérielle peuvent entraîner ou aggraver une hypotension artérielle, notamment orthostatique. L'arrêt simultané des bêtabloquants et des antihypertenseurs d'action centrale peut aggraver le rebond d'hypertension artérielle qui suit l'arrêt brutal de la clonidine et le propranolol doit être arrêté plusieurs jours avant l'arrêt de la clonidine.
Médicaments non cardiovasculaires
Corticoïdes
Les patients avec un hémangiome infantile peuvent présenter un risque accru d'hypoglycémie s'ils ont reçu ou s'ils reçoivent simultanément un traitement par corticoïdes car la suppression surrénalienne pourrait entraîner un défaut de réponse à l'hormone de contre-régulation, le cortisol, et ainsi majorer le risque d'hypoglycémie. Ceci s'applique également aux enfants allaités par leur mère traitée par corticoïdes en cas de posologies élevées ou de traitement prolongé.
Médicaments induisant une hypotension orthostatique
Ces médicaments peuvent induire une hypotension artérielle posturale (dérivés nitrés, inhibiteurs de la phosphodiestérase de type 5, antidépresseurs tricycliques, antipsychotiques, agonistes dopaminergiques, lévodopa, amifostine, baclofène …) qui pourra être aggravée si co-administrés au propranolol. Il convient de demander l'avis d'un cardiologue.
Chlorpromazine
Une administration concomitante du propranolol avec la chlorpromazine peut entraîner une augmentation des concentrations plasmatiques des deux substances. Ceci peut se manifester avec un effet anti-psychique plus fort de la chlorpromazine et un effet anti-hypertenseur plus fort du propranolol.
Sympathicomimétiques
Une administration concomitante de sympathicomimétiques, par exemple d'adrénaline, peut antagoniser l'effet des bêtabloquants. L'administration parentérale de médicaments contenant de l'adrénaline peut entraîner chez les patients sous bêtabloquants dans des cas rares une vasoconstriction, une hypertension et une bradycardie.
Ergotamine
Il convient d'être prudent en cas de co-administration de propranolol avec de l'ergotamine, de la dihydro-ergotamine et autres substances apparentés. Une combinaison pareille a provoqué dans des cas isolés des réactions vasospastiques.
Hypoglycémiants
Tous les bêtabloquants peuvent masquer certains symptômes de l'hypoglycémie: palpitations et tachycardie.
Il convient d'être prudent en cas d'utilisation concomitante de propranolol avec un traitement hypoglycémiant chez les patients diabétiques car cela pourrait prolonger la réponse hypoglycémique à l'insuline. Dans ce cas, prévenir le personnel soignant et renforcer, surtout en début de traitement, la surveillance glycémique.
Hypolipémiants
L'administration concomitante de cholestyramine ou de colestipol avec le propranolol peut entraîner une diminution allant jusqu'à 50% des concentrations de propranolol.
Anesthésiques halogénés
Ils peuvent diminuer la contractilité myocardique et la réponse vasculaire compensatoire en cas d'administration avec le propranolol. Les bêta-stimulants peuvent être utilisés pour contrer le bêta-blocage.
Substrats ou inhibiteurs du CYP2D6
L'administration concomitante de substrats ou inhibiteurs du CYP2D6, comme amiodarone, cimétidine, fluoxétine, paroxétine, quinidine et ritonavir peut augmenter la toxicité et la concentration sanguine du propranolol. Aucune interaction n'a été observée avec la ranitidine ou le lansoprazole.
Substrats ou inhibiteurs du CYP1A2
L'administration concomitante de substrats ou inhibiteurs du CYP1A2, comme amiodarone, imipramine, cimétidine, ciprofloxacine, fluvoxamine, isoniazide, théophylline, zileuton, zolmitriptan et rizatriptan peut augmenter la toxicité et la concentration sanguine du propranolol.
Rizatriptan
L'administration concomitante de rizatriptan et propranolol peut provoquer une augmentation d'environ 70-80% de l'AUC et de la Cmax du rizatriptan. L'exposition accrue au rizatriptan est probablement provoquée par l'inhibition du métabolisme de premier passage hépatique (monoamine oxydase-A) du rizatriptan. Un ajustement de la dose de rizatriptan sera nécessaire dans le cas d'une prescription concomitante des deux médicaments.
Substrats ou inhibiteurs du CYP2C19
L'administration concomitante de substrats ou inhibiteurs du CYP2C19, comme fluconazole, cimétidine, fluoxétine, fluvoxamine, téniposide et tolbutamide peut augmenter la toxicité et la concentration sanguine du propranolol. Aucune interaction n'a été observée avec l'oméprazole.
Inducteurs du métabolisme médicamenteux
Après l'administration concomitante d'inducteurs comme la rifampicine, l'éthanol, la phénytoïne et le phénobarbital, les taux sanguins de propranolol peuvent être diminués.
Grossesse/Allaitement
Non pertinent.
Mères qui allaitent: voir «Mises en garde et précautions» et «Interactions».
Effet sur l’aptitude à la conduite et l’utilisation de machines
Non pertinent.
Effets indésirables
Résumé du profil de tolérance
Dans les essais cliniques conduits dans les hémangiomes infantiles prolifératifs, les effets indésirables les plus fréquemment rapportés chez les enfants traités par Hemangiol ont été des troubles du sommeil, des infections respiratoires majorées telles que bronchite et bronchiolite associées à une toux et une fièvre, des diarrhées et des vomissements.
La sécurité d'Hemangiol chez les patients âgés de >1 an n'a pas été étudiée.
Globalement, les effets indésirables rapportés au cours du programme d'autorisation temporaire d'utilisation et dans la littérature ont été des hypoglycémies (et les événements associés tels que des crises convulsives hypoglycémiques) et des infections respiratoires majorées associées à une détresse respiratoire.
Le tableau suivant présente les effets indésirables rapportés, quelles que soient la dose et la durée du traitement, dans deux études cliniques conduites chez 424 patients traités par Hemangiol à la dose de 1 mg/kg/jour ou de 3 mg/kg/jour sur une durée maximale de traitement de 6 mois.
La fréquence des effets indésirables est définie en utilisant la convention suivante: très fréquent (≥1/10); fréquent (≥1/100 à <1/10); peu fréquent (≥1/1000 à <1/100); rare (≥1/10'000 à <1/1000); très rare (<1/10'000); fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Compte tenu de la taille de la base de données des essais cliniques, les catégories Rare et Très rare ne sont pas représentées.
Au sein de chaque classe de systèmes d'organes, les effets indésirables sont présentés par ordre décroissant de gravité.
Système de classes d'organes | Très fréquent | Fréquent | Peu fréquent | Fréquence indéterminée |
Infections et infestations | Bronchite | Bronchiolite | ||
Troubles du métabolisme et de la nutrition | Diminution de l'appétit | |||
Affections psychiatriques | Troubles du sommeil | Agitation Cauchemars Irritabilité | ||
Affections du système nerveux | Somnolence | Crise convulsive hypoglycémique | ||
Affections cardiaques | Bloc AV | Bradycardie | ||
Affections vasculaires | Extrémités froides | Hypotension artérielle Vasoconstriction Syndrome de Raynaud | ||
Affections respiratoires, thoraciques et médiastinales | Bronchospasme | |||
Affections gastro-intestinales | Diarrhées Vomissements | Constipation Douleurs abdominales | ||
Affections de la peau et du tissu sous-cutané | Erythème Erythème fessier | Urticaire Alopécie | Dermatite psoriasiforme | |
Investigations | Diminution de la pression artérielle | Diminution de la glycémie Diminution de la fréquence cardiaque Neutropénie | Agranulocytose Hyperkaliémie |
Description de certains effets indésirables
Concernant les infections des voies respiratoires inférieures telles que la bronchite ou la bronchiolite, une aggravation des symptômes (y compris de bronchospasme) a été observée chez des patients traités par Hemangiol en raison de l'effet bronchoconstricteur du propranolol. Ces effets ont dans de rares cas conduit à l'arrêt définitif du traitement (voir «Mises en garde et précautions»).
Les troubles du sommeil recouvrent l'insomnie, un sommeil de mauvaise qualité et l'hypersomnie. Les autres affections du système nerveux central ont principalement été observées en début de traitement.
Des diarrhées ont été fréquemment rapportées sans être systématiquement associées à une maladie gastro-intestinale infectieuse. La survenue de diarrhées semble dose-dépendante entre 1 et 3 mg/kg/jour. Aucun cas n'a été d'intensité sévère ni n'a conduit à l'arrêt du traitement.
Les événements cardiovasculaires rapportés au cours des études cliniques ont été asymptomatiques. Lors des 4 heures de surveillance cardiovasculaire réalisée pendant les jours de titration, une diminution de la fréquence cardiaque (d'environ 7 bpm) et de la pression artérielle systolique (<3 mm Hg) a été observée après l'administration du médicament. Un cas de bloc cardiaque auriculoventriculaire du second degré chez un patient avec des troubles de la conduction sous-jacents a entraîné l'arrêt définitif du traitement. Des cas isolés de bradycardie symptomatique et d'hypotension artérielle ont été rapportés dans la littérature.
Les baisses de la glycémie observées au cours des études cliniques ont été asymptomatiques. Toutefois, plusieurs cas d'hypoglycémie associée à une crise convulsive hypoglycémique ont été rapportés au cours du programme d'autorisation temporaire d'utilisation et dans la littérature, notamment en cas de jeûne lors d'une maladie concomitante (voir «Mises en garde et précautions»).
Le traitement concomitant par corticoïdes systémiques peut majorer le risque d'hypoglycémie (voir «Mises en garde et précautions»).
Une hyperkaliémie a été rapportée dans la littérature chez quelques patients avec un hémangiome ulcéré étendu (voir «Mises en garde et précautions»).
Fertilité
Bien que certains effets réversibles sur la fertilité des mâles et des femelles aient été rapportés dans la littérature chez des rats adultes recevant de fortes doses de propranolol, l'étude réalisée chez de jeunes animaux n'a pas montré d'effet sur la fertilité.
Déclaration des effets indésirables suspectés
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
Surdosage
La toxicité des bêtabloquants est une extension de leurs effets thérapeutiques:
- Les symptômes cardiaques de sévérité légère à modérée sont une diminution de la fréquence cardiaque et une hypotension artérielle. Des blocs auriculoventriculaires, des retards de conduction intraventriculaire et une insuffisance cardiaque congestive peuvent se produire en cas de toxicité plus sévère.
- Un bronchospasme peut se développer, en particulier chez les patients asthmatiques.
- Une hypoglycémie peut se développer et les manifestations d'hypoglycémie (tremblement, tachycardie) peuvent être masquées par d'autres effets cliniques de toxicité des bêtabloquants.
Le propranolol est fortement liposoluble et il peut traverser la barrière hémato-encéphalique et provoquer des crises convulsives.
Soutien et traitement:
Le patient doit être placé sous monitorage cardiaque et sous surveillance des signes vitaux, de l'état mental et de la glycémie. Des liquides en intraveineux en cas d'hypotension artérielle et de l'atropine en cas de bradycardie doivent être administrés. L'administration de glucagon puis de catécholamines doit être envisagée si le patient ne répond pas de manière appropriée aux liquides en intraveineux. L'isoprotérénol et l'aminophylline peuvent être utilisés en cas de bronchospasme.
Propriétés/Effets
Code ATC
C07AA05
Mécanisme d'action
Les mécanismes d'action potentiels du propranolol dans l'hémangiome infantile prolifératif décrits dans la littérature pourraient inclure divers mécanismes imbriqués les uns aux autres:
- un effet hémodynamique local (vasoconstriction, conséquence classique du blocage des récepteurs bêta-adrénergiques, donc diminution de la perfusion de l'hémangiome);
- un effet anti-angiogénique (diminution de la prolifération des cellules endothéliales vasculaires, réduction de la néo-vascularisation et de la formation des tubules vasculaires, réduction de la sécrétion de la métalloprotéinase de la matrice 9);
- un effet inducteur d'apoptose sur les cellules endothéliales capillaires;
- une réduction des voies de signalisation de VEGF et bFGF donc de l'angiogenèse/prolifération.
Pharmacodynamique
Le propranolol est un bêtabloquant caractérisé par trois propriétés pharmacologiques:
- absence d'activité bêtabloquante bêta-1 cardiosélective,
- effet antiarythmique,
- absence de pouvoir agoniste partiel (ou d'activité sympathomimétique intrinsèque).
Efficacité clinique
L'efficacité du propranolol chez l'enfant (âgé de 5 semaines à 5 mois lors de l'instauration du traitement) avec un hémangiome infantile prolifératif nécessitant un traitement systémique a été démontrée dans une étude pivotale adaptative de phase II/III, multicentrique, randomisée, contrôlée, en doses multiples, destinée à comparer quatre protocoles de traitement de propranolol (1 ou 3 mg/kg/jour pendant 3 ou 6 mois) versus placebo (double aveugle).
Le traitement a été administré à 456 sujets (401 propranolol à la dose de 1 ou 3 mg/kg/jour pendant 3 ou 6 mois; 55 placebo), avec une phase de titration de 3 semaines. Les patients (71,3% de sexe féminin; 37% âgés de 35 à 90 jours et 63% âgés de 91 à 150 jours) présentaient un hémangiome cible au niveau de la tête pour 70% d'entre eux et les hémangiomes étaient en majorité des hémangiomes localisés (89%).
Le succès du traitement était défini comme la résolution complète ou quasi complète de l'hémangiome cible, qui a été déterminée par des évaluations indépendantes centralisées en aveugle des photographies à la semaine 24, en l'absence d'arrêt prématuré du traitement.
Le protocole de traitement 3 mg/kg/jour pendant 6 mois (sélectionné à la fin de la partie de phase II de l'étude) a permis d'obtenir un taux de succès de 60,4% versus 3,6% dans le groupe placebo (p <0,0001). L'analyse en sous-groupes définis en fonction de l'âge (35‑90 jours/91-150 jours), du sexe et de la localisation de l'hémangiome (tête/corps) n'a pas identifié de différences dans la réponse au propranolol. Une amélioration de l'hémangiome a été observée après 5 semaines de traitement par le propranolol chez 88% des patients. 11,4% des patients ont dû être retraités après l'arrêt du traitement.
Pour des raisons éthiques liées à l'utilisation du placebo, la démonstration de l'efficacité n'a pas été établie chez les patients présentant un hémangiome à haut risque. Des preuves de l'efficacité du propranolol chez les patients avec un hémangiome à haut risque sont disponibles aussi bien dans la littérature que dans le cadre d'un programme spécifique d'autorisation temporaire d'utilisation d'Hemangiol.
Sur la base d'une étude rétrospective, une minorité de patients (12%) a nécessité la reprise d'un traitement systémique. Lors de la reprise du traitement, une réponse satisfaisante a été observée chez une grande majorité de patients.
Pharmacocinétique
Absorption:
Le propranolol est presque complètement absorbé après administration orale. Il subit toutefois un effet de premier passage hépatique important et, en moyenne, seulement 25% environ du propranolol atteint la circulation systémique. La concentration plasmatique maximale est obtenue en 1 à 4 heures environ après administration par voie orale. L'administration d'aliments riches en protéines augmente la biodisponibilité du propranolol d'environ 50%, sans modification du temps d'obtention de la concentration maximale.
Le propranolol est un substrat pour le transporteur d'efflux intestinal P-glycoprotéine (P-gp). Des études suggèrent toutefois que la P-gp n'est pas dose-limitante pour l'absorption intestinale du propranolol dans l'intervalle des doses thérapeutiques habituelles.
Distribution
Environ 90% du propranolol circulant sont liés aux protéines plasmatiques (albumine et glycoprotéine alpha-1 acide). Le volume de distribution du propranolol est d'environ 4 l/kg. Le propranolol traverse la barrière hémato-encéphalique et la barrière placentaire et il se retrouve dans le lait maternel.
Métabolisme:
Le propranolol est métabolisé par trois voies principales: hydroxylation aromatique (principalement 4-hydroxylation), N-désalkylation suivie d'une oxydation des chaînes latérales et glucuroconjugaison directe. Les contributions en pourcentage de ces voies au métabolisme total sont respectivement de 42%, 41% et 17%, mais avec une variabilité considérable entre individus. Les quatre métabolites finaux majeurs sont le propranolol glucuronidé, l'acide naphtyloxylactique, l'acide glucuronique et les sulfoconjugués du 4-hydroxypropranolol. Les études in vitro ont indiqué que le CYP2D6 (hydroxylation aromatique), le CYP1A2 (oxydation des chaînes) et, dans une moindre mesure, le CYP2C19 sont impliqués dans le métabolisme du propranolol. Le 4-hydroxypropanolol est un inhibiteur faible de CYP2D6.
Élimination
Chez les sujets sains, aucune différence concernant la clairance orale ou la demi-vie d'élimination n'a été observée entre les métaboliseurs rapides et les métaboliseurs lents du CYP2D6.
La demi-vie d'élimination plasmatique du propranolol est comprise entre 3 et 6 heures. Moins de 1% de la dose est excrétée sous forme inchangée dans les urines.
Cinétique pour certains groupes de patients
Enfants et adolescents
La pharmacocinétique d'Hemangiol a été étudiée chez 19 enfants âgés de 35 à 150 jours. La concentration plasmatique maximale à l'équilibre a généralement été mesurée 2 heures après administration avec 3 mg/kg/jour en 2 prises.
La valeur moyenne correspondante était d'environ 79 ng/ml, quel que soit l'âge de l'enfant.
La clairance rénale apparente moyenne a été de 2,71 l/h/kg chez les enfants âgés de 65 à 120 jours et de 3,27 l/h/kg chez les enfants âgés de 181 à 240 jours. Une fois corrigés en fonction du poids corporel, les principaux paramètres pharmacocinétiques du propranolol (tels que la clairance plasmatique) déterminés chez les enfants ont été similaires à ceux rapportés dans la littérature pour les adultes.
Le métabolite 4-hydroxy-propranolol a été quantifié, l'exposition plasmatique à ce métabolite a été de moins de 7% en comparaison avec l'exposition à la molécule mère.
Données précliniques
Les principaux effets rapportés après administration répétée de propranolol chez des rats adultes et des rats jeunes ont été une diminution transitoire du poids corporel.
Sur la base de l'ensemble des données in vitro et in vivo disponibles, on peut conclure que le propranolol est dépourvu de potentiel génotoxique.
Les études d'administration avec l'alimentation, dans lesquelles des souris et des rats ont été exposés à du chlorhydrate de propranolol jusqu'à 18 mois à des doses allant jusqu'à 150 mg/kg/jour, n'ont mis en évidence aucun effet carcinogène lié au médicament.
Chez des rats femelles adultes, l'administration dans l'utérus ou l'injection du propranolol a empêché l'implantation à une dose ≥4 mg par animal.
Chez les rats mâles adultes, l'administration répétée de propranolol à forte dose (≥7,5 mg/kg) a induit des lésions histopathologiques des testicules, des épididymes et des vésicules séminales, une diminution de la motilité des spermatozoïdes, de la concentration des spermatozoïdes et des taux plasmatiques de testostérone ainsi qu'une augmentation significative des anomalies des spermatozoïdes. Les effets ont généralement été réversibles après l'arrêt du traitement. Des résultats similaires ont été obtenus après l'administration intra-testiculaire de propranolol ainsi que dans des modèles in vitro.
Les effets potentiels du propranolol sur le développement des rats jeunes ont été évalués après administration orale quotidienne de doses de 0, 10, 20 ou 40 mg/kg/jour à partir du jour post-natal 4 (JPN4) jusqu'à JPN21.
Une mortalité ainsi qu'une diminution réversible de la prise du poids ont été observées à la dose de 40 mg/kg/jour, conduisant à une NOAEL de 20 mg/kg/jour pour la toxicité juvénile.
En termes de croissance, de développement corporel et neurologique et fonction reproductrice, il n'y a eu aucun effet lié au propranolol jusqu'à la dose maximale.
Cela correspondant à des marges de sécurité de 1,2 chez les femelles et de 2,9 chez les mâles, sur la base des expositions moyennes au propranolol à JPN21.
Remarques particulières
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Stabilité après ouverture: 2 mois
Le flacon ne doit pas être agité avant utilisation
Remarques particulières concernant le stockage
Conserver Hemangiol dans le récipient fermé dans l'emballage d'origine et hors de portée des enfants à température ambiante (15-25°C) pour le protéger de la lumière. Le médicament ne doit pas être congelé.
Une seringue pour administration orale graduée en mg de propranolol base est fournie avec le flacon.
Numéro d’autorisation
61214 (Swissmedic).
Titulaire de l’autorisation
Pierre Fabre (Suisse) SA, 4123 Allschwil.
Mise à jour de l’information
Septembre 2020.
Reviews (0)
Recently Viewed

Free consultation with an experienced pharmacist
Describe the symptoms or the right drug - we will help you choose its dosage or analogue, place an order with home delivery or just consult.
We are 14 pharmacists and 0 bots. We will always be in touch with you and will be able to communicate at any time.

 Deutsch
Deutsch French
French Italian
Italian