Tisseel 2ml Doppelka Fertigspritze (dss) buy online
Tisseel Lös 2ml Doppelkammer Fertigspritzen (Dual Syringe System
-
510.22 CHF
- Price in reward points: 3131

- Availability: Not available
- Product Code: 5440407
- ATC-code B02BC30
- EAN 7680526180214
Ingredients:
Aprotinin 2250-3750, Nicotinamid, Natriumchlorid, Histidin, Blutgerinnungsfaktor IIa human (Thrombin human) 400-625 UI, Blutgerinnungsfaktor XIII 0.6-10 UI, Albumin human, Blutgerinnungsfaktor I (human) 72-110 mg, Polysorbat 80, Calciumchlorid-2-Wasser, Natriumcitrat-2-Wasser, Wasser für Injektionszwecke 1 ml.

Description
Zusammensetzung
Kleberprotein-Lösung:
Wirkstoffe: Fibrinogenum humanum, Factor XIII, Aprotininum syntheticum
Hilfsstoffe: Albuminum humanum, L-Histidinum, Nicotinamidum, Natrii citras dihydricum, Polysorbatum 80 (Tween 80), Aqua ad iniectabilia
Thrombin-Lösung:
Wirkstoffe: Thrombinum humanum, Calcii chloridum dihydricum
Hilfsstoffe: Albuminum humanum, Natrii chloridum, Aqua ad iniectabilia
Galenische Form und Wirkstoffmenge pro Einheit
Fibrinkleber, tiefgefroren.
Die Kleberprotein-Lösung enthält pro ml:
Fibrinogen (als clottierbares Protein) 72 - 1101 mg
Aprotinin (synthetisch) 3000 KIE2
Faktor XIII 0.6 – 10 IE3
Die Thrombin-Lösung enthält pro ml:
Thrombin 500 IE4
Calciumchlorid Dihydrat 40 µmol (5.88 mg)
1 Enthalten in einer Gesamtprotein-Konzentration von 110.5 mg/ml
2 1 EPU (European Pharmacopeia Units) entspricht 1800 KIE (Kallidogenase-Inaktivator-Einheiten)
31 Einheit (IE) Faktor XIII entspricht jener Aktivität, die in 1 ml frischem Normalplasma enthalten ist
4Die Thrombin-Aktivität wird gemäss dem aktuellen internationalen WHO-Standard für Thrombin ermittelt
Indikationen/Anwendungsmöglichkeiten
TISSEEL unterstützt die Blutstillung, wenn chirurgische Standardtechniken nicht ausreichen.
TISSEEL ist ein Fibrinkleber zur Klebung und Abdichtung von Geweben, oder zur Sicherung von chirurgischen Nähten in der Gefässchirurgie oder bei gastrointestinalen Anastomosen. Ausserdem dient TISSEEL der Klebung und Abdichtung von Geweben und der Nahtsicherung in der Neurochirurgie und bei chirurgischen Eingriffen, bei denen es zum Kontakt mit Liquor, Dura Mater kommen kann, wie beispielsweise otologische, rhinologische, ophthalmische und vertebrale Eingriffe.
Bei der Anwendung von TISSEEL wird zum Teil auch biokompatibles Material wie z.B. Kollagenvlies als Träger- und Verstärkermaterial eingesetzt.
Dosierung/Anwendung
TISSEEL darf nur von erfahrenen Chirurgen angewendet werden, die in der Anwendung von TISSEEL geschult wurden.
Dosierung
Das erforderliche Volumen an TISSEEL-Lösung richtet sich nach der Grösse der zu klebenden oder zu beschichtenden Fläche bzw. nach der Grösse des auszufüllenden Defektes. Ausserdem ist es von der gewählten Applikationsmethode abhängig.
Die bei der Erstapplikation auf eine anatomische Struktur bzw. Zielfläche eingesetzte Menge sollte ausreichen, um den betreffenden Bereich vollständig abzudecken.
Die Anwendung kann bei Bedarf wiederholt erfolgen. Eine Wiederanwendung von TISSEEL auf eine bestehende polymerisierte TISSEEL Schicht sollte jedoch vermieden werden, da TISSEEL auf einer polymerisierten Schicht nicht klebt.
Bei der Klebung von Flächen kann als Anhaltspunkt dienen, dass die Packungsgrösse TISSEEL 2,0 ml (d.h. 1 ml Kleberprotein-Lösung und 1 ml Thrombin-Lösung zu gleichen Teilen) für eine Fläche von mindestens 10 cm² ausreicht.
Wird der Fibrinkleber durch Sprühen appliziert, so kann mit der gleichen Menge (d.h. 1 ml Kleberprotein-Lösung und 1 ml Thrombin-Lösung) je nach Indikation eine Fläche von 25 bis 100 cm² beschichtet werden.
Verabreichungen ausserhalb der vorgesehenen Applikationsfläche sollten vermieden werden.
TISSEEL nur als dünne Schicht auftragen. Ein zu dickes Fibringerinnsel kann sich auf die Wirksamkeit des Produkts und die Wundheilung auswirken.
TISSEEL wurde bei Früh- wie Neugeborenen, Kleinkindern bis hin zu Jugendlichen, zum Teil in grösserer Zahl angewendet; dies gilt insbesondere für die Gebiete Lebertransplantation, Oesophagus/Trachea (besonders bei Fisteln), Herzchirurgie, Urogenitalbereich, Bauchhöhle/Darm, sowie Nervenanastomosen.
Die Anwendung und Sicherheit bei Kindern und Jugendlichen ist bis jetzt nicht geprüft worden.
Art der Anwendung
Zur topischen Anwendung auf der Wundfläche. Nicht injizieren.
Um optimale Sicherheit bei der Anwendung von TISSEEL zu gewährleisten, sollen die folgenden Empfehlungen befolgt werden:
Bei offener Chirurgie soll ein Druckregelgerät verwendet werden, dessen Maximaldruck höchstens 2,0 bar (28,5 psi) beträgt.
Bei minimal invasiven/laparoskopischen Eingriffen soll ein Druckregelgerät verwendet werden, dessen Maximaldruck höchstens 1,5 bar (22 psi) beträgt und das ausschliesslich Kohlendioxidgas verwendet.
Vor dem Aufbringen von TISSEEL muss die Wundoberfläche mittels Standardtechniken (z.B. intermittierende Anwendung von Kompressen, Tupfern, Anwendung von Saugern) getrocknet werden. Verwenden Sie keine Druckluft oder Gas um die Applikationsstelle zu trocknen. TISSEEL darf nur auf sichtbare Applikationsstellen gesprüht werden.
TISSEEL darf nur gemäss den Anweisungen und unter Verwendung der Produkte und Geräte rekonstituiert bzw. verabreicht werden, die für dieses Produkt empfohlen werden (siehe “Hinweise zur Handhabung“).
Für die Sprühapplikation siehe “Warnhinweise und Vorsichtmassnahmen” und “Hinweise zur Handhabung” mit besonderen Empfehlungen zum erforderlichen Druck und Gewebeabstand je nach Art des Eingriffs und zur Länge der Applikationshilfen.
Unmittelbar vor der Anwendung sollten die ersten Tropfen von der Applikationskanüle ausgeschieden und verworfen werden, um die Verwendung eines ausreichend vermischten Präparates sicherzustellen.
Kontraindikationen
TISSEEL alleine ist nicht indiziert zur Behandlung von massiven arteriellen und venösen Blutungen.
TISSEEL darf nicht intravaskulär angewendet werden. Eine intravaskuläre Anwendung kann lebensbedrohliche thromboembolische Ereignisse zur Folge haben. Bei Überempfindlichkeit gegenüber einem der Wirkstoffe oder sonstigen Bestandteile, sowie bei bekannter Überempfindlichkeit gegen Rinderprotein oder synthetisches Aprotinin, darf TISSEEL nicht angewendet werden.
Eine Injektion in die Nasenschleimhaut darf nicht erfolgen, da hier schwerwiegende allergisch-anaphylaktoide Reaktionen aufgetreten sind und es zu thromboembolischen Komplikationen im Versorgungsbereich der Arteria ophthalmica kommen kann.
Warnhinweise und Vorsichtsmassnahmen
Nur zur Anwendung auf Wundflächen. Nicht intravaskulär anwenden.
Bei Patienten mit allergischer Diathese oder Arzneimittelüberempfindlichkeit sowie bei Patienten, die Aprotinin bereits in der Vergangenheit erhalten haben, ist eine sorgfältige Risiko/Nutzen-Abwägung erforderlich. Es empfiehlt sich, Antihistaminika vor der Gabe von Aprotinin zu verabreichen.
Bei der Injektion von Kleberprotein- und/oder Thrombin-Lösungen in Weichteilgewebe besteht das Risiko einer anaphylaktischen Reaktion.
Wie bei allen Proteinprodukten sind allergische Überempfindlichkeitsreaktionen nicht ausgeschlossen.
TISSEEL sollte nicht intravaskulär angewendet werden, da dies zu anaphylaktischen Reaktionen und / oder thromboembolischen Komplikationen führen kann, die beide lebensbedrohlich sein können.
Eine intravaskuläre Anwendung kann die Wahrscheinlichkeit und den Schweregrad von akuten Überempfindlichkeitsreaktionen bei empfindlichen Patienten erhöhen.
Zeichen auf Überempfindlichkeitsreaktionen sind: Bradykardie, Tachykardie, Hypotonie, Hitzegefühl, Bronchspasmus, Giemen, Dyspnoe, Übelkeit, Urtikaria, Angioödem, Pruritus, Erythem, Parästhesie. Es wurde auch über schwerwiegende anaphylaktische Reaktionen, einschliesslich anaphylaktischer Schock mit TISSEEL berichtet (siehe Unerwünschte Wirkungen).
Bei Auftreten eines dieser Symptome ist die Anwendung unverzüglich abzubrechen und die derzeit gültigen Standardmassnahmen für eine Schockbehandlung einzuleiten.
Bereits appliziertes Präparat muss von der Applikationsstelle entfernt werden.
TISSEEL enthält synthetisches Aprotinin, ein monomerisches Polypeptid das bekannt ist, mit dem Risiko von anaphylaktischen Reaktionen im Zusammenhang zu stehen. Auch bei strikt lokaler Anwendung besteht das Risiko von anaphylaktischen Reaktionen auf Aprotinin, insbesondere im Fall einer vorangegangenen Exposition.
Deshalb sollte jede Verwendung von Aprotinin oder aprotininhaltigen Präparaten in der Krankenakte vermerkt werden.
Da synthetisches Aprotinin die identische Struktur wie das bovine Aprotinin aufweist, sollte die Anwendung von TISSEEL bei Patienten mit Allergien gegen Rinderproteine sorgfältig abgewogen werden.
In zwei retrospektiven, nicht randomisierten Studien in der koronaren Bypass-Chirurgie zeigten Patienten, die Fibrinkleber erhielten ein statistisch signifikant erhöhtes Mortalitätsrisiko. Obwohl diese Studien keinen kausalen Zusammenhang belegen, kann ein Zusammenhang zwischen dem erhöhten Risiko und der Verabreichung von TISSEEL nicht ausgeschlossen werden. Um eine unerwünschte intravasale Verabreichung zu vermeiden, ist daher besondere Vorsicht geboten.
Bei der Verabreichung von Fibrinklebern mit einem Sprühgerät ist Vorsicht geboten.
TISSEEL soll nur als dünne Schicht aufgetragen werden. Eine zu dicke Schicht kann die Wirksamkeit des Produkts und die Wundheilung negativ beeinflussen.
Bei der Verwendung von Sprühgeräten mit Druckgasreglern zur Verabreichung von TISSEEL sind lebensbedrohliche/tödliche Luft- oder Gasembolien aufgetreten. Dieses Ereignis scheint mit der Verwendung von Spray-Sets mit höherem als dem empfohlenen Druck und/oder mit einem zu geringen Abstand zur Gewebeoberfläche zusammenzuhängen. Das Risiko scheint höher zu sein, wenn Fibrinkleber mit Luft aufgesprüht werden, als beim Sprühen mit CO2 und ist daher beim Aufsprühen von TISSEEL auf offene Operationswunden nicht auszuschliessen.
Wird TISSEEL mittels Sprühapplikation aufgetragen, muss sichergestellt werden, dass ein Druck verwendet wird, der im vom Hersteller des Sprühgeräts empfohlenen Druckbereich liegt (siehe Tabelle unter „Hinweise zur Handhabung“ für Drücke und Abstände).
TISSEEL darf nur per Sprühapplikation verabreicht werden, wenn der Sprühabstand exakt beurteilt werden kann. Nicht näher als im empfohlenen Abstand aufsprühen.
Beim Aufsprühen von TISSEEL sollen Änderungen von Blutdruck, Puls, Sauerstoffsättigung und endexspiratorischem CO2 überwacht werden, da die Möglichkeit einer Luft- oder Gasembolie besteht (siehe auch „Dosierung/Anwendung“).
TISSEEL darf nicht mit dem Easy Spray / Spray Set System in geschlossenen Körperbereichen angewendet werden.
Ohne zusätzliche blutstillende Massnahmen ist TISSEEL Fibrinkleber nicht zur Behandlung von massiven und starken arteriellen Blutungen indiziert.
Kleberprotein- und/oder Thrombin-Lösungen, die bei der Anwendung auf Gewebe ausserhalb des zu klebenden Bereichs gelangt sind, sollten nach Möglichkeit entfernt werden. Vor der Verwendung von TISSEEL müssen alle Körperteile ausserhalb der zu behandelnden Fläche sorgfältig abgedeckt werden, um eine Gewebeadhäsion an einer unerwünschten Stelle zu vermeiden.
Werden Fibrinkleber in geschlossen Bereichen angewendet, besteht das Risiko von Kompressionskomplikationen.
TISSEEL Fibrinkleber wird aus humanem Plasma hergestellt. Standardmassnahmen zur Verhinderung von Infektionen, die sich durch den Einsatz von Arzneimitteln ergeben, die aus Blut oder Blutplasma hergestellt werden, schliessen die Auswahl der Spender und das Screening der einzelnen Spenden und Plasmapools auf spezifische Infektionsmarker sowie den Einsatz effektiver Schritte zur Inaktivierung / Entfernung von Viren im Herstellungsverfahren ein. Dennoch kann bei der Verabreichung von Arzneimitteln aus menschlichem Blut oder Blutplasma die Möglichkeit der Übertragung von Krankheitserregern nicht völlig ausgeschlossen werden. Dies gilt auch für bislang unbekannte oder neu aufgetretene Viren und andere Pathogene.
Die ergriffenen Sicherheitsmassnahmen werden als wirksam gegen umhüllte Viren wie z.B. HIV, HBV und HCV sowie gegen das unbehüllte Hepatitis A Virus (HAV) betrachtet. Für Parvovirus B19 können die getroffenen Massnahmen von eingeschränktem Wert sein.
Parvovirus B19 Infektionen können schwerwiegende Folgen für schwangere Frauen (fötale Infektion) und für Personen mit Immunmangelkrankheiten oder gesteigerter Erythropoese (z.B. hämolytische Anämie) haben.
Es wird empfohlen, bei jeder Verabreichung von TISSEEL Fibrinkleber an einen Patienten den Namen und die Chargennummer des Präparates zu dokumentieren, um einen Zusammenhang zwischen Patient und Produktcharge herzustellen.
Während der Herstellung von TISSEEL wird Heparin (aus Schweinemucosa) als Hilfsstoff verwendet. Im Endprodukt ist kein Heparin mehr nachweisbar.
Oxidierte Cellulose-haltige Präparate können die Wirksamkeit von TISSEEL vermindern und sollten deshalb nicht als Trägermaterial eingesetzt werden (siehe «Sonstige Hinweise»)
Interaktionen
Es wurden keine formalen Wechselwirkungsstudien durchgeführt.
Alkohol-, jod- oder schwermetallhaltige Lösungen interferieren wegen der Denaturierung von Proteinen oder anderen Mechanismen mit der Wirksamkeit des Präparates. Deshalb sollten diese Substanzen vor der Anwendung von TISSEEL Fibrinkleber weitestmöglich entfernt werden.
TISSEEL Fibrinkleber kann auch bei voll heparinisierten Patienten, z.B. bei extrakorporalem Kreislauf, angewendet werden.
Schwangerschaft/Stillzeit
Die Sicherheit der Anwendung von Fibrinklebern während der Schwangerschaft und Stillzeit wurde nicht in kontrollierten klinischen Studien untersucht.
Es liegen keine hinreichenden tierexperimentellen Studien zur Auswirkung auf Schwangerschaft, Embryonalentwicklung, Entwicklung des Fötus und/oder die postnatale Entwicklung vor. Daher, und weil ein Gehalt an Parvovirus B19 in TISSEEL nicht kategorisch ausgeschlossen werden kann (siehe “Warnhinweise und Vorsichtsmassnahmen“) sollte das Medikament in der Schwangerschaft und während der Stillzeit nicht angewendet werden.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Nicht zutreffend.
Unerwünschte Wirkungen
In seltenen Fällen können bei Patienten, die mit Fibrinkleber/Hämostatika behandelt werden, Überempfindlichkeitsreaktionen oder allergische Reaktionen auftreten (z.B. Angioödeme, Brennen und Stechen am Verabreichungsort, Bradykardie, Bronchospasmus, Schüttelfrost, Atemnot, Hautrötungen (Flush), generalisierte Urtikaria, Kopfschmerzen, Nesselsucht, Hypotonie, Lethargie, Übelkeit, Juckreiz, Ruhelosigkeit, Tachykardie, Engegefühl in der Brust, Kribbeln, Erbrechen, Stenoseatmung).
In Einzelfällen sind diese Reaktionen bis zur schweren Anaphylaxie fortgeschritten. Solche Reaktionen können besonders dann beobachtet werden, wenn das Präparat wiederholt oder bei Patienten angewendet wird, bei denen bereits früher eine Überempfindlichkeit gegenüber Aprotinin, Rinderproteine (siehe „Warnhinweise und Vorsichtsmassnahmen“) oder einen anderen Bestandteil des Präparats aufgetreten ist.
Selbst wenn eine erste Behandlung mit TISSEEL gut vertragen wurde, kann eine weitere Anwendung des Präparats oder die systemische Anwendung von Aprotinin schwere anaphylaktische Reaktionen zur Folge haben.
In seltenen Fällen können sich Antikörper gegen Bestandteile des Fibrinklebers bilden.
Intravaskuläre Verabreichung kann zu thromboembolischen Komplikationen führen, und es besteht ein Risiko anaphylaktischer Reaktionen.
Speziell bei koronaren Bypass-Operationen sollte TISSEEL mit Vorsicht angewendet werden, um jegliches Risiko der intravaskulären Anwendung zu minimieren.
Hinweise zur Sicherheit in Bezug auf übertragbare Erreger siehe „Warnhinweise und Vorsichtsmassnahmen“.
In klinischen Studien und aus der post-marketing surveillance (markiert mit einem p in der nachfolgenden Auflistung) mit Baxter Fibrinkleber wurde über folgende unerwünschten Wirkungen mit TISSEEL berichtet.
In den klinischen Studien wurde TISSEEL als Zusatzhämostatikum in der Kardio-, Vaskular-, Hüftgelenkersatz-, Leber- und Milz-Chirurgie verabreicht. Andere klinische Studien schlossen die Klebung von Lymphgefässen in Patienten mit axillärer Lymphknotenentfernung, Klebung von Kolon-Anastomosen und Duraklebung in der hinteren Schädelgrube ein. Da die Häufigkeit von unerwünschten Wirkungen, welche aus der Post-Marketing-Surveillance berichtet wurden, anhand der vorhandenen Daten nicht abgeschätzt werden kann, wurde, wenn immer möglich, die obere Grenze des 95% Konfidenzintervalls unter Anwendung des Dreisatzes wie folgt berechnet: 3/1146 = 0.0026 oder 0.26% d.h. gelegentlich (wobei «1146» die totale Anzahl Patienten ist, die in klinischen Studien mit TISSEEL behandelt wurden).
Sehr häufig (≥ 1/10), häufig (≥ 1/100 bis <1/10), gelegentlich (≥ 1/1,000 bis <1/100), selten (≥ 1/10,000 bis <1/1,000), sehr selten (<1/10,000), unbekannt (kann nicht anhand der vorhandenen Daten geschätzt werden).
Allgemeine Bereiche | Nebenwirkung | Häufigkeit |
Infektionen und parasitäre Erkrankungen | Postoperative Wundinfektion | häufig |
Störungen des Blutes und des Lymphsystems | Erhöhung von Fibrinabbauprodukten | gelegentlich |
Störungen des Immunsystems | Überempfindlichkeitsreaktionen* p | gelegentlich |
Anaphylaktische Reaktionen* p | gelegentlich | |
Anaphylaktischer Schock* p | gelegentlich | |
Parästhesie p | gelegentlich | |
Bronchospasmus p | gelegentlich | |
Giemen p | gelegentlich | |
Pruritus p | gelegentlich | |
Erythem p | gelegentlich | |
Störungen des Nervensystems | Sensorische Missempfindungen | häufig |
Funktionsstörungen des Herzens | Bradykardie p | gelegentlich |
Tachykardie p | gelegentlich | |
Funktionsstörungen der Gefässe | Achselvenenthrombose ** | häufig |
Hypotonie | selten | |
Hämatome p | gelegentlich | |
Arterielle Embolie p | gelegentlich | |
Luftembolie*** p | unbekannt | |
Embolie der Zerebralarterien p | gelegentlich | |
Zerebralinfarkt** p | gelegentlich | |
Respiratorische, thorakale und mediastinale Funktionsstörungen | Dyspnoe p | gelegentlich |
Gastrointestinale Beschwerden | Übelkeit | gelegentlich |
Intestinale Obstruktion p | gelegentlich | |
Funktionsstörungen der Haut und des Unterhautgewebes | Hautausschlag | häufig |
Urtikaria p | gelegentlich | |
Gestörte Wundheilung p | gelegentlich | |
Störungen der Skelettmuskulatur und des Bindegewebes | Gliederschmerzen | häufig |
Allgemeine Störungen und Reaktionen an der Applikationsstelle | Schmerzen | häufig |
Erhöhte Körpertemperatur | häufig | |
Hautrötung p | gelegentlich | |
Ödeme p | gelegentlich | |
Verletzungen und Vergiftungen | Postprozeduale Schmerzen | gelegentlich |
Serom | sehr häufig | |
Angioödem p | gelegentlich |
* anaphylaktische Reaktionen und anaphylaktischer Schock schliessen tödliche Reaktionen ein.
** als Folge intravaskulärer Applikation im Sinus petrosus superior.
*** wie mit anderen Fibrinklebern sind auch unter TISSEEL bei der Verwendung von Druckgas lebensbedrohliche/tödliche Luft- und Gasembolien aufgetreten. Diese Ereignisse scheinen mit einer unsachgemässen Anwendung von Sprühgeräten im Zusammenhang zu stehen (z.Bsp. mit einem höheren Druck als empfohlen und in unmittelbarer Nähe der Gewebsoberfläche).
p unerwünschte Wirkungen aus der post-marketing surveillance.
Klasseneffekte
Andere Nebenwirkungen, welche mit Fibrinkleber/Hämostatika assoziiert werden, schliessen Überempfindlichkeitsreaktionen ein, welche sich durch Reizung an der Applikationsstelle, Brustkorbbeschwerden, Schüttelfrost, Kopfschmerz, Lethargie, Unruhe und Erbrechen manifestieren können.
Überdosierung
Der Fibrinkleber sollte nur als dünne Schicht aufgetragen werden, da zu dicke Schichten die Wirksamkeit des Präparates und den Wundheilungsprozess stören können.
Eigenschaften/Wirkungen
ATC-Code: B02BC30
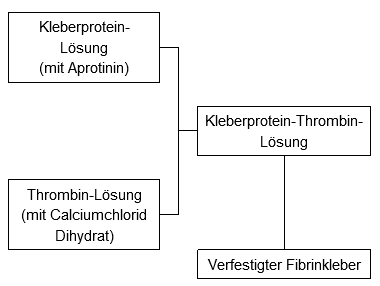
TISSEEL Fibrinkleber ist ein biologischer Zweikomponentenkleber. Die beiden Komponenten liegen tiefgefroren vor und müssen vor der Anwendung aufgetaut werden. Während oder unmittelbar vor der Anwendung werden die beiden Komponenten (Kleberprotein-Lösung und Thrombin-Lösung) vermischt (siehe Applikationsmethoden). Es entsteht eine viskose Kleberprotein-Thrombin-Lösung, die rasch zu einer weissen, elastischen Masse wird, welche fest am Gewebe haftet. Die Verfestigung läuft analog der physiologischen Gerinnung ab und dient zur Blutstillung, zum Wundverschluss sowie zur Gewebeklebung. Im Verlauf der Wundheilung kommt es zu einer vollständigen Resorption des verfestigten Fibrinklebers.
Das folgende Schema soll den Ablauf verdeutlichen:
Pharmakokinetik
Die Fibrinklebung führt analog zur letzten Stufe der natürlichen Blutgerinnung innerhalb weniger Minuten zur Ausbildung eines physiologischen Fibringerüstes. Dieses Gerüst in Form eines dreidimensionalen Netzwerkes wird in der Folge von Fibroblasten besiedelt. Die einsetzende Kollagensynthese der Fibroblasten führt zur bindegewebigen Organisation des Wundgebietes.
Gleichzeitig kommt es zu einer allmählichen Resorption des Fibrins, wobei histomorphologisch kein Unterschied zum Abbau körpereigenen, extravasalen Fibrins feststellbar ist. Die Geschwindigkeit des Fibrinabbaus wird einerseits durch die fibrinolytische Aktivität des umgebenden Gewebes und die eingewanderten Granulozyten, andererseits durch die Menge des dem Kleber zugesetzten Fibrinolyseinhibitors Aprotinin beeinflusst. Das im TISSEEL in geringer Menge vorhandene Plasminogen wird unter Einwirkung von Plasminogen-Aktivatoren aus dem umgebenden Gewebe in Plasmin überführt, welches Fibrin zu löslichen Spaltprodukten (FDP) abbaut. Die Fibrinspaltprodukte werden durch die neben den Fibroblasten in das Wundgebiet eingewanderten Granulozyten und Makrophagen phagozytiert und weiter abgebaut.
Thrombin bildet einen Komplex mit Antithrombin III. Dieser Komplex und Aprotinin werden proteolytisch abgebaut, während das CaCl2 dem Elektrolythaushalt zugeführt wird.
Aufgrund der pharmakokinetischen Profile konnte Bioäquivalenz von bovinem und synthetischem Aprotinin gezeigt werden.
Präklinische Daten
TISSEEL mit (bovinem oder synthetischem) Aprotinin hat sich in in-vivo-Studien inklusive solcher zur Wundheilung bei Ratten und Kaninchen als gut verträglich erwiesen.
In humanen Fibroblasten-Kulturen zeigte die Kleberproteinlösung von TISSEEL hervorragende Zellkompatibilität bei fehlender Zytotoxizität. Darüberhinaus konnte in geeigneten In vitro-Tests keine Mutagenität nachgewiesen werden.
Subkutane akute Toxizitätsstudien an Ratten und Kaninchen zeigten keine akute Toxizität von TISSEEL bei guter lokaler Verträglichkeit. Synthetisches und bovines Aprotinin wurden selbst nach einmaliger intravenöser und paravenöser Applikation sehr hoher Dosen (bis 1'500'000 IU/kg bei Ratte oder Maus toleriert. Die beobachteten No-Observed_Adverse-Event-Effect Level wurden mit <100'000 IU/kg (Maus) und <200'000 IU/kg (Ratte) bestimmt. In geeigneten Meerschweinchen-Modellen gab es weder Anzeichen für sensibilisierendes noch für anaphylaktisches Potential von synthetischem oder bovinem Aprotinin.
Basierend auf einer systematischen Literaturanalyse können auf für TISSEEL verwendeten Lösungsmitteln / Detergentien / Reagentien beruhende Nebenwirkungen oder Toxizitäten ausgeschlossen werden.
Sonstige Hinweise
Inkompatibilitäten
Oxidierte Zellulose-haltige Präparate können die Wirksamkeit von TISSEEL vermindern und sollten deshalb nicht als Trägermaterial eingesetzt werden.
TISSEEL darf nicht mit anderen Arzneimitteln gemischt werden.
Alkohol-, jod- oder schwermetallhaltige Lösungen interferieren wegen der Denaturierung von Proteinen oder anderen Mechanismen mit der Wirksamkeit des Präparates. Lässt sich deren Verwendung nicht vermeiden, so sind etwaige Reste vor Beginn der Klebung möglichst vollständig zu entfernen.
Haltbarkeit
Das Medikament darf nur bis zu dem auf dem Behälter mit ''Exp:'' bezeichneten Datum verwendet werden.
Die aufgetauten Lösungen innerhalb von höchstens 72 Stunden nach dem Auftauen verwenden. Bis zum Gebrauch bei Raumtemperatur (15 – 25 °C) in ungeöffneter und unbeschädigter Sterilverpackung lagern.
Nach dem Auftauen nicht mehr einfrieren und nicht im Kühlschrank lagern!
Besondere Lagerungshinweise
Tiefgekühlt (≤-20 °C) lagern. Die Kühlkette bis zur Anwendung nicht unterbrechen.
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
Für Kinder unerreichbar aufbewahren!
Hinweise für die Handhabung
Allgemeines
Vor der Verwendung von TISSEEL müssen alle Körperteile ausserhalb der zu behandelnden Fläche sorgfältig abgedeckt werden, um eine Gewebeadhäsion an einer unerwünschten Stelle zu vermeiden.
Um ein Haftenbleiben des Fibrinklebers zu vermeiden, Handschuhe und Instrumente, die mit Kleberprotein-Thrombin-Lösung in Berührung kommen können, vorher mit steriler Kochsalzlösung anfeuchten.
Eine separate, sequentielle Anwendung der beiden Komponenten muss vermieden werden. Das heisst beide Komponenten müssen gemeinsam aufgetragen werden und dürfen nicht getrennt appliziert werden.
Vorbereitung und Rekonstitution
Die Kleberprotein- und Thrombinlösung befinden sich je in einer Fertigspritze zum Einmalgebrauch. Das Präparat wurde unter aseptischen Bedingungen in zwei sterilen Beuteln verpackt. Der innere Beutel und dessen Inhalt sind steril, solange die äussere Verpackung unbeschädigt ist.
Es wird empfohlen, beide Kleberkomponenten in einem sterilen Wasserbad bei
33 °C – 37 °C aufzutauen und zu erwärmen. Das Wasserbad darf eine Temperatur von 37 °C nicht überschreiten (um den vorgegebenen Temperaturbereich zu überwachen die Wassertemperatur mit einem Thermometer kontrollieren und gegebenenfalls das Wasser wechseln. Wird ein steriles Wasserbad für das Auftauen und Erwärmen verwendet, die Fertigspritze aus den Beuteln entnehmen).
Die Schutzkappe der Spritze erst nach vollständigem Auftauen entfernen und die Applikationsnadel sofort aufsetzen. TISSEEL nicht anwenden, bis die Lösungen vollständig aufgetaut sind.
Das Auftauen und Erwärmen der Fertigspritze kann nach einer der vier folgenden Methoden vorgenommen werden:
1. Schnelles Auftauen / Erwärmen (steriles Wasserbad) – empfohlene Methode
Den inneren Beutel in den Sterilbereich bringen, die Fertigspritze aus dem Innenbeutel entnehmen und direkt in das sterile Wasserbad legen. Sicherstellen, dass der Inhalt der Fertigspritze vollständig in das Wasser eingetaucht ist.
Tabelle 1: Auftau- und Erwärmungszeiten im sterilen Wasserbad bei 33 °C
bis maximal 37 °C
Packungsgrösse | Mindestzeit für Auftauen und Erwärmen auf 33 °C bis maximal 37 °C im |
PRIMA-Spritze | |
2 ml | 5 Minuten |
4 ml | 5 Minuten |
2. Auftauen / Erwärmen in einem nicht sterilen Wasserbad
Als Alternative kann das Präparat ausserhalb des sterilen Bereiches unter Anwendung eines nicht sterilen Wasserbads aufgetaut werden.
Hierzu die Fertigspritze in den beiden Beuteln belassen und für die entsprechende Dauer in ein Wasserbad ausserhalb des Sterilbereiches legen (siehe Tabelle 2). Sicherstellen, dass die Beutel während der gesamten Auftaudauer in das Wasser eingetaucht bleiben. Nach dem Auftauen aus dem Wasserbad entnehmen, den Aussenbeutel trocknen und den Innenbeutel mit der Fertigspritze in den Sterilbereich bringen.
Tabelle 2: Auftau- und Erwärmzeiten in einem nicht sterilen Wasserbad bei 33 °C bis maximal 37 °C
Packungsgrösse | Mindestzeit für Auftauen- und Erwärmen auf 33 °C bis maximal 37 °C im nicht sterilen Wasserbad |
PRIMA-Spritze | |
2 ml | 15 Minuten |
4 ml | 20 Minuten |
3. Auftauen und Erwärmen in einem Inkubator
Alternativ können die Kleberkomponenten auch in einem Inkubator bei 33 - 37 °C aufgetaut und erwärmt werden.
Die Auftau- und Erwärmungszeiten im Inkubator sind in Tabelle 3 angegeben. Bei diesen Angaben wird davon ausgegangen, dass sich das Produkt in den Beuteln befindet.
Tabelle 3: Auftau- und Erwärmungszeiten im Inkubator von 33 °C bis maximal 37 °C
Packungsgrösse | Mindestzeit für Auftauen- und Erwärmen auf 33 °C bis maximal 37 °C, im Inkubator |
PRIMA-Spritze | |
2 ml | 40 Minuten |
4 ml | 50 Minuten |
4) Auftauen bei Raumtemperatur (nicht über +25 °C) / Erwärmen vor der Anwendung in einem Inkubator auf 33 °C – 37 °C
Das Präparat kann bei Raumtemperatur aufgetaut werden. Die in Tabelle 4 angeführten Zeitangaben sind Minimalzeiten für das Auftauen bei Raumtemperatur. Nach dem Auftauen ist das Präparat bei Raumtemperatur zu lagern und muss innerhalb von 72 Stunden verwendet werden.
Wenn das Auftauen bei Raumtemperatur erfolgt, muss das Präparat kurz vor Gebrauch zusätzlich in einem Inkubator auf 33 °C – 37 °C erwärmt werden. Die entsprechenden Erwärmungszeiten sind ebenfalls in Tabelle 4 angeführt.
Tabelle 4: Auftau- und Erwärmungszeiten bei Raumtemperatur (RT), gefolgt von einem zusätzlichen Erwärmen vor Gebrauch im Inkubator bei 33 °C bis maximal 37 °C.
Packungs-grösse | Mindestzeit für Auftauen bei Raumtemperatur (nicht über 25 °C), gefolgt von einem zusätzlichen Erwärmen vor der Anwendung in einem Inkubator bei 33° bis maximal 37 °C (Präparat in Beuteln) | |
PRIMA Spritze | ||
Auftauzeiten bei Raumtemperatur | Erwärmzeiten im Inkubator | |
2 ml | 80 Minuten | + 11 Minuten |
4 ml | 90 Minuten | + 13 Minuten |
–Das Produkt zum Auftauen nicht in den Händen halten!
–Nicht in die Mikrowelle geben!
–Nach dem Auftauen nicht in den Kühlschrank geben und nicht wieder einfrieren!
Bei Raumtemperatur aufgetaute ungeöffnete Beutel können bei kontrollierter Raumtemperatur (nicht über +25 °C) bis zu 72 Stunden gelagert werden. Wird das Präparat nicht innerhalb von 72 Stunden nach dem Auftauen verwendet, muss es verworfen werden.
Um eine optimale Vermischung der beiden Lösungen zu erzielen, müssen die beiden Kleberkomponenten unmittelbar vor der Anwendung auf 33–37 °C erwärmt werden. TISSEEL darf nicht Temperaturen über 37 °C exponiert werden und nicht in die Mikrowelle gegeben werden.
Die Kleberproteinlösung und die Thrombinlösung sollten klar bis leicht opaleszierend sein. Lösungen, die trüb sind oder Ablagerungen aufweisen, nicht verwenden. Die aufgetauten Präparate vor der Anwendung visuell auf Schwebstoffe und Verfärbungen überprüfen.
Die aufgetaute Kleberproteinlösung sollte eine leicht viskose Flüssigkeit sein. Wenn die Lösung die Konsistenz eines verfestigten Gels aufweist, ist davon auszugehen, dass sie denaturiert wurde (z.B. aufgrund einer Unterbrechung der Kühlkette oder durch Überhitzen während des Erwärmens). In diesem Fall darf TISSEEL nicht angewendet werden.
Die Spritze erst kurz vor der Anwendung aus dem Beutel entnehmen. Die Spritzenschutzkappen erst zur Anwendung von den Spritzen entfernen.
Bei der PRIMA-Spritze soll um das Entfernen der Schutzkappe zu erleichtern, zuerst die Spritzenkappe hin-und her bewegt werden. Erst dann die Schutzkappe abziehen.
TISSEEL erst verwenden, wenn das Präparat vollständig aufgetaut und auf 33° bis 37° Grad erwärmt ist (flüssige Konsistenz).
Zu weiteren Anweisungen für die Vorbereitung bitte das zuständige Krankenpflegepersonal oder den Arzt befragen.
Verabreichung mit der PRIMA-Spritze
Für die Applikation die Doppelkammer-Fertigspritze mit der Kleberprotein- und der Thrombin-Lösung an ein Anschluss-Stück und eine Applikationskanüle anschliessen, die im Set mit dem Applikationszubehör mitgeliefert wurden. Die Doppelkolbenstange der Doppelkammer-Fertigspritze stellt sicher, dass gleiche Mengen der Kleberkomponenten über das Anschluss-Stück in die Applikationskanüle gelangen, wo sie gemischt und anschliessend aufgetragen werden.
Arbeitsanleitung für die Handhabung der PRIMA-Spritze
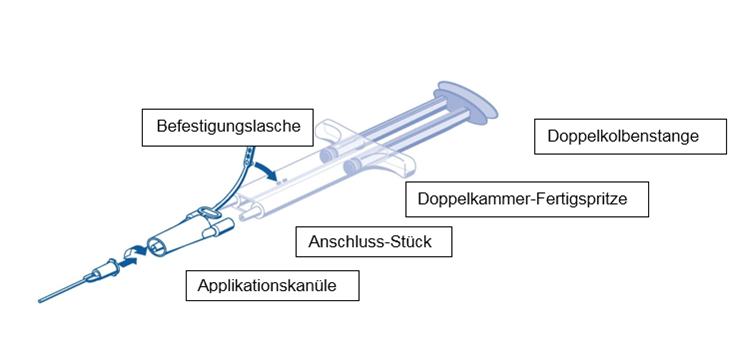
1.Spritze vor dem Anbringen der Applikationsteile vollständig entlüften.
2.Das Anschluss-Stück und die Befestigungslasche an der Seite der Spritze mit dem Befestigungsloch für die Befestigungslasche ausrichten.
3.Die Konusse der Doppelkammer-Fertigspritze mit dem Anschluss-Stück verbinden. Dabei auf festen Halt achten.
Das Anschluss-Stück mit der Befestigungslasche an der Doppelkammer-Fertigspritze fixieren.
Wenn die Befestigungslasche reisst, das mitgelieferte Ersatz-Anschluss-Stück verwenden.
Wenn das Ersatz-Anschluss-Stück nicht vorhanden ist, kann das System trotzdem verwendet werden, sofern sorgfältig darauf geachtet wird, dass die Verbindung fest sitzt und dicht ist.
Nicht die Luft im Anschluss-Stück herausdrücken.
4.Eine Applikationskanüle auf das Anschluss-Stück stecken. Die Luft im Anschluss-Stück und in der Applikationskanüle erst bei Beginn der eigentlichen Applikation mit herausdrücken, da sonst die Applikationskanüle verstopfen könnte.
Hinweis: Vor der Anwendung von TISSEEL muss die Wundoberfläche mit Standardtechniken (z.B. mehrmaliges Aufdrücken von Kompressen oder Tupfern, Verwendung von Sauggeräten) getrocknet werden. Zum Trocknen keine Druckluft und kein Gas verwenden.
Die gemischte Kleberprotein-Thrombin-Lösung auf die vorgesehene Oberfläche oder auf die Flächen der zu verklebenden Teile durch Ausüben von Druck auf die Rückseite der Doppelkolbenstange auftragen.
Bei chirurgischen Eingriffen, die das Auftragen eines Mindestvolumens des Fibrinklebers verlangen, wird empfohlen, die ersten Tropfen des Produkts herauszudrücken und zu verwerfen.
Nach Auftragen von TISSEEL mindestens 2 Minuten vergehen lassen, um eine ausreichende Polymerisation zu erzielen.
Wenn die Applikation der Fibrinkleberkomponenten unterbrochen wird, kann es unmittelbar zu einer Verstopfung der Kanüle kommen. Die Applikationskanüle in diesem Falle erst unmittelbar vor der Fortsetzung der Applikation gegen eine neue austauschen. Sollten die Austrittsöffnungen des Anschluss-Stücks verstopft sein, das mitgelieferte Ersatz-Anschluss-Stück verwenden.
Hinweis:
Wegen der hohen Konzentration der Thrombin-Lösung (500 I.E./ml) setzt die Verfestigung des Fibrinklebers innerhalb von Sekunden nach Vermischung ein.
Der Fibrinkleber kann auch mit anderem von Baxter gelieferten Zubehör aufgetragen werden, das sich besonders für beispielsweise den endoskopischen Einsatz, die minimal-invasive Chirurgie oder die Applikation auf grosse oder schwer zugängliche Flächen eignet. Beim Einsatz solcher Applikationshilfen bitte genau nach Bedienungsanleitung vorgehen.
Nach der Applikation von TISSEEL mindestens 2 Minuten warten, um eine genügende Polymerisation zu erhalten.
Bei der Anwendung von TISSEEL wird zum Teil auch biokompatibles Material wie z.B. Kollagenvlies als Träger- und Verstärkermaterial eingesetzt.
Wird TISSEEL mit Hilfe eines Sprühgeräts aufgetragen, muss sichergestellt werden, dass der Druck und der Gewebeabstand innerhalb der folgenden, vom Hersteller empfohlenen Bereiche liegen:
Empfohlener Druck, Gewebeabstand und Sprühgeräte für die Applikation von TISSEEL | |||||
Art der Chirurgie | Zu verwendendes Sprühset | Zu verwendende Applikationshilfe | Zu verwendender Druckregler | Empfohlener Abstand vom Zielgewebe | Empfohlener Sprühdruck |
Offene Wunde | Tisseel / Artiss Spray Set | n. z. | EasySpray | 10-15 cm | 1,5-2,0 bar |
Tisseel / Artiss Spray Set 10er-Pack | n. z. | EasySpray | |||
Laparoskopie/ minimal invasive Eingriffe | n. z. | Duplospray MIS Applikator 20 cm | Duplospray MIS Regulator | 2–5 cm | 1,2-1,5 bar (18-22 psi) |
Duplospray MIS Regulator NIST B11 | |||||
Duplospray MIS Applikator 30 cm | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Duplospray MIS Applikator 40 cm | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Austauschbare Spitze | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Beim Aufsprühen von TISSEEL sollen Änderungen von Blutdruck, Puls, Sauerstoffsättigung und endexspiratorischem CO2 überwacht werden, da die Möglichkeit einer Luft- oder Gasembolie besteht (siehe „Dosierung/Anwendung“ und „Warnhinweise und Vorsichtsmassnahmen“).
Zulassungsnummer
52'618 (Swissmedic)
Zulassungsinhaberin
Baxter AG, 8152 Opfikon
Stand der Information
Januar 2018
Composition
Solution de colle de protéine:
Principes actifs : Fibrinogenum humanum, Factor XIII, Aprotininum syntheticum
Excipients: Albuminum humanum, L-Histidinum, Nicotinamidum, Natrii citras dihydricum, Polysorbatum 80 (Tween 80), Aqua ad iniectabilia
Solution de thrombine:
Principes actifs: Thrombinum humanum, Calcii chloridum dihydricum
Excipients: Albuminum humanum, Natrii chloridum, Aqua ad iniectabilia
Forme galénique et quantité de principe actif par unité
Colle de fibrine, congelée
1 ml de solution de colle de protéine contient:
Fibrinogène (protéine coagulable) 72 – 110 mg1
Aprotinine (synthétique) 3000 UIK2
Facteur XIII 0.6 – 10 UI3
1 ml de solution de thrombine contient:
Thrombine 500 UI4
Dihydrate de chlorure de calcium 40 µmol (5.88 mg)
1 Contenus dans une concentration de protéine totale de 110.5 mg/ml
2 1 EPU (European Pharmacopoeia Units) correspond à 1800 unités inhibitrices de la kallicréine UIK.
3 1 unité (UI) de facteur XIII correspond à l'activité contenue dans 1 ml de plasma frais normal
4 L'activité de la thrombine est déterminée selon le standard international actuel de l'OMS
Indications/Possibilités d’emploi
TISSEEL soutient l'hémostase là où les techniques chirurgicales ne suffisent pas.
TISSEEL est une colle de fibrine utilisée pour le collage et l'étanchement des tissus, pour la protection des sutures en chirurgie vasculaire ou des anastomoses gastro-intestinales. En outre TISSEEL sert au collage et à l'étanchement des tissus ainsi qu'à la protection de la suture dans la neurochirurgie et lors d'interventions chirurgicales impliquant un contact avec le liquide céphalo-rachidien, la dure-mère, comme par exemple les interventions otologiques, rhinologiques, ophtalmiques ou vertébrales.
TISSEEL est parfois utilisée aussi en association avec des matériaux biocompatibles, par exemple les compresses de collagène qui servent de soutien et de renforcement.
Posologie/Mode d’emploi
L'utilisation de TISSEEL est réservée aux chirurgiens expérimentés qui ont reçu une formation à l'utilisation de TISSEEL.
Posologie
Le volume requis de solution de TISSEEL est fonction soit de l'étendue de la surface à coller ou à enduire, soit de l'étendue de la perte de substance à combler. Il dépend en outre de la méthode d'application choisie.
La quantité initiale de produit à appliquer sur un site anatomique donné ou sur une surface cible doit être suffisante pour couvrir entièrement le site d'application prévu.
L'application peut être répétée si nécessaire.
Eviter cependant de réutiliser TISSEEL sur une couche polymérisée existante de TISSEEL, car TISSEEL n'adhère pas sur une telle couche.
Pour le collage de surfaces, on peut prendre comme point de repère qu'un conditionnement de TISSEEL 2,0 ml (c.-à-d. 1 ml de solution de colle de protéine et 1 ml de solution de thrombine, à parts égales) suffit pour une surface d'au moins 10 cm².
Lorsque la colle de fibrine est appliquée par pulvérisation, cette même quantité (c.-à-d. 1 ml de solution de colle de protéine et 1 ml de solution de thrombine) permet d'enduire, selon l'indication, une surface de 25 à 100 cm².
Des administrations au dehors de la surface d'application prévue doivent être évitées.
TISSEEL doit être appliqué qu'en couche fine. Une épaisseur excessive du caillot de TISSEEL pourrait avoir un effet sur l'efficacité du produit et le processus de cicatrisation.
Dans plusieurs cas, TISSEEL a été utilisé chez les nouveau-nés et prématurés, les enfants en bas âge jusqu'à chez les adolescents; ceci est notamment valable pour les domaines de transplantation hépatique, œsophage/trachée (spécialement lors de fistules), chirurgie cardiaque, région urogénitale, cavité abdominale/intestin ainsi que anastomoses nerveuses.
L'utilisation et la sécurité d'emploi n'ont pas à ce jour été étudiées chez l'enfant et l'adolescent.
Mode d'emploi
À usage topique sur la surface de la lésion. Ne pas injecter.
Les recommandations suivantes doivent être respectées pour garantir une sécurité optimale lors de l'application de TISSEEL:
En chirurgie ouverte, il convient d'utiliser un dispositif de contrôle de la pression assurant une pression maximum de 2,0 bars (28,5 psi).
Lors d'interventions peu invasives/laparoscopiques, il convient d'utiliser un dispositif de contrôle de la pression assurant une pression maximum de 1,5 bar (22 psi) et fonctionnant exclusivement à l'aide de gaz carbonique.
Avant d'appliquer TISSEEL, la surface de la plaie doit être séchée à l'aide des techniques standard (p.ex. application intermittente de compresses, d'écouvillons, utilisation de dispositifs d'aspiration). N'utilisez pas d'air comprimé ou de gaz pour sécher le site d'application. TISSEEL ne doit être pulvérisé que sur des sites d'application visibles.
TISSEEL ne doit être reconstitué et administré que conformément aux instructions et avec les dispositifs recommandés pour ce produit (voir "Remarques concernant la manipulation").
Pour l'application par pulvérisation, voir "Mises en garde et précautions" et "Remarques concernant la manipulation" pour des recommandations spécifiques concernant la pression à appliquer et la distance à respecter avec le tissu en fonction de la procédure chirurgicale et de la longueur des embouts applicateurs.
Juste avant l'emploi, faire sortir et jeter les premières gouttes de la canule d'application, afin d'assurer l'utilisation d'un produit suffisamment mélangé.
Contre-indications
TISSEEL seul n'est pas indiqué pour le traitement d'hémorrragies artérielles et veineuses massives.
TISSEEL ne doit pas être appliqué par voie intravasculaire. Des complications thrombo-emboliques mettant en jeu le pronostic vital peuvent survenir en cas d'application intravasculaire.
TISSEEL ne doit pas être appliqué en cas d'hypersensibilité à l'un des principes actifs ou à des autres composants, ainsi qu'en cas d'hypersensibilité connue aux protéines bovines ou à l'aprotinine synthétique.
Eviter toute injection dans la muqueuse nasale, car on a constaté dans ce cas des réactions allergiques-anaphylactoïdes très graves et il peut en résulter des complications thromboemboliques dans la zone irriguée par l'artère ophtalmique.
Mises en garde et précautions
Pour application épilésionelle uniquement. Ne pas utiliser par voie intravasculaire.
Il faut soigneusement mettre en balance les risques et les avantages chez les patients présentant une diathèse allergique ou une hypersensibilité au médicament, ainsi que chez les patients ayant déjà reçu auparavant de l'aprotinine. Il est recommandé d'administrer des antihistaminiques avant de donner de l'aprotinine.
Lors de l'injection de la solution de colle de protéine et/ou thrombine dans les tissus mous il existe un risque de réaction anaphylactique. Comme pour tout produit d'origine protéique, des réactions allergiques d'hypersensibilité sont possibles.
TISSEEL ne devrait pas être utilisé par voie intravasculaire car ceci peut provoquer des réactions anaphylactiques et/ou des complications thromboemboliques, risquant de mettre la vie en danger. Chez les patients susceptibles, une application intravasculaire peut augmenter la probabilité et la sévérité des réactions acutes d'hypersensibilité.
Signes de réactions d'hypersensibilité sont: bradycardie, tachycardie, hypotension, bouffée congestive, bronchospasme, sibilances, dyspnée, nausées, urticaire, angioedème, prurit, érythème, paresthésie. Des réactions anaphylactiques graves, y compris choc anaphylactique ont été rapportées avec TISSEEL (voir "Effets indésirables").
En cas d'apparition d'un de ces symptômes, l'administration doit être interrompue immédiatement et les mesures standard actuelles pour un traitement de choc doivent être initiées.
Eliminer tout produit déjà appliqué de la zone d'application.
TISSEEL contient de l'aprotinine synthétique, un polypeptide monomérique connu pour être associé à des réactions anaphylactiques. Même en cas d'application strictement locale, il existe un risque de réaction anaphylactique liée à la présence d'aprotinine, notamment en cas d'une exposition antérieure.
En conséquence, toute application d'aprotinine ou de produits à base d'aprotinine doit donc être consignée dans le dossier du patient.
L'aprotinine synthétique ayant une structure identique à celle de l'aprotinine bovine, l'utilisation de TISSEEL doit être étroitement surveillée chez les patients allergiques aux protéines bovines.
Dans deux études rétrospectives et non-randomisées dans la chirurgie de pontage coronaire, une augmentation significative du risque de mortalité à été enregistrée chez les patients ayant reçus la colle de fibrine. Bien que ces études ne montrent pas de lien de causalité, on ne peut pas exclure une causalité entre l'augmentation du risque et l'application de TISSEEL. Pour éviter une administration intra-vasculaire, une prudence particulière s'impose.
La prudence est recommandée lors de l'application des colles de fibrine à l'aide d'un dispositif de pulvérisation.
TISSEEL ne doit être appliqué qu'en couche fine. Une épaisseur de caillots excessive peut perturber l'efficacité du produit et le processus de guérison des lésions.
Une embolie gazeuse fatale/mettant en jeu le pronostic vital est survenue en cas d'utilisation de dispositifs de pulvérisation munis d'un dispositif de contrôle de la pression pour administrer TISSEEL. Cet événement semble être lié à l'utilisation du dispositif de pulvérisation à une pression supérieure à celle recommandée et/ou à proximité de la surface du tissu. Le risque semble être plus élevé lorsque les colles de fibrine sont pulvérisées à l'air qu'au CO2 et ne peut donc être exclu lorsque TISSEEL est pulvérisé dans le cadre d'une intervention ouverte.
Lors de l'application de TISSEEL à l'aide d'un dispositif de pulvérisation, veiller à utiliser une pression conforme aux limites recommandées par le fabricant du dispositif (voir tableau sous "Remarques concernant la manipulation" pour une liste des pressions et des distances).
TISSEEL ne doit être appliqué par pulvérisation que s'il est possible d'évaluer précisément la distance de pulvérisation, conformément aux recommandations du fabricant. Ne pas pulvériser à des distances inférieures à celles recommandées.
Lors de la pulvérisation de TISSEEL, il convient de surveiller tout changement de pression artérielle, de fréquence cardiaque, de saturation en oxygène et de CO2 de fin d'expiration en raison du risque d'embolie gazeuse (voir également "Posologie/Mode d'emploi").
TISSEEL ne peut pas être utilisé avec le système Easy Spray / Spray Set dans des régions du corps enfermées.
Sans mesure hémostatique supplémentaire, la colle de fibrine TISSEEL n'est pas indiquée pour traiter des hémorragies artérielles massives et fortes.
Lors de l'utilisation sur un tissu, il faut éliminer le plus possible les solutions de colle de protéine et/ou de thrombine ayant débordé de la zone à traiter.
Avant d'appliquer TISSEEL, couvrir soigneusement toutes les parties du corps non concernées par l'application, pour éviter une adhésion tissulaire sur des sites non souhaités.
Il existe un risque de complications compressives, si les colles de fibrine sont appliquées dans des régions enfermées.
La colle de fibrine TISSEEL est produite à partir de plasma humain. Les mesures habituelles de prévention du risque de transmission d'agents infectieux par les médicaments préparés à partir de sang ou de plasma humain comprennent la sélection des donneurs, la recherche de marqueurs spécifiques d'infection sur chaque don et sur les pools de plasma et l'inclusion dans le procédé de fabrication d'étapes efficaces pour l'inactivation/élimination virale.
Cependant, lorsque des médicaments préparés à partir de sang ou de plasma humain sont administrés, le risque de transmission d'agents infectieux ne peut pas être totalement exclu. Ceci s'applique également aux virus inconnus ou émergents ou autres types d'agents infectieux.
Les mesures de sécurité prises sont considérées comme efficaces contre les virus enveloppés tels que VIH, VHB et VHC ainsi que contre le virus non enveloppé de l'hépatite A (VHA). Les mesures prises peuvent être d'efficacité limitée vis-à-vis du parvovirus B19.
L'infection par le parvovirus B19 peut être grave chez les femmes enceintes (infection foetale) et chez les sujets immunodéprimés ou présentant une augmentation de la production de globules rouges (par ex. anémie hémolytique).
Lors de chaque administration de la colle de fibrine TISSEEL à un patient, il est recommandé de documenter le nom et le numéro de lot de la préparation pour pouvoir établir un rapport entre le patient et le lot du produit.
De l'héparine (produite à partir de muqueuse porcine) est utilisée comme adjuvant au cours de la fabrication de TISSEEL. L'héparine n'est plus décelable dans le produit fini.
Des produits contenant de cellulose oxydée peuvent réduire l'efficacité de TISSEEL. Pour cette raison ces produits ne devraient pas être utilisés comme matériau porteur (voir "Remarques particulières").
Interactions
Aucune étude formelle d'interaction n'a été réalisée.
A cause de la dénaturation des protéines ou d'autres mécanismes des solutions contenant de l'alcool, de l'iode ou des métaux lourds interfères avec l'efficacité du produit. C'est pourquoi il faut éliminer le plus possible ces substances avant l'utilisation de la colle de fibrine TISSEEL.
La colle de fibrine TISSEEL peut aussi être utilisée chez les patients à héparinisation complète, par ex. en cas de circulation extracorporelle.
Grossesse/Allaitement
La sécurité d'emploi des colles de fibrine pendant la grossesse et l'allaitement n'a pas été étudiée dans des études cliniques contrôlées.
Il n'existe pas d'expérimentations animales suffisantes concernant l'incidence sur la grossesse, le développement embryonnaire, le développement fœtal, et/ou le développement postnatal. Pour cette raison et parce que une teneur de parvovirus B19 dans le TISSEEL ne peut pas être exclue catégoriquement (voir «Mises en garde et précautions»), le médicament ne devra pas être utilisé pendant la grossesse et l'allaitement.
Effet sur l’aptitude à la conduite et l’utilisation de machines
Non pertinent.
Effets indésirables
Des réactions d'hypersensibilité ou allergiques (pouvant inclure: œdème de Quincke, brûlures et démangeaisons au site d'application, bradycardie, bronchospasme, frissons, dyspnée, bouffée congestive, urticaire généralisée, mal de tête, urticaire, hypotension, léthargie, nausée, prurit, agitation, tachycardie, oppression thoracique, picotements, vomissements, respiration sifflante) peuvent survenir dans de rares cas chez des patients traités par des colles de fibrine/substances hémostatiques.
Dans des cas isolés, ces réactions ont évolué vers une anaphylaxie grave. De telles réactions peuvent particulièrement être observées si la préparation est appliquée de manière répétée ou administrée à des patients ayant des antécédents d'hypersensibilité à l'aprotinine, aux protéines d'origine bovines ou à d'autres composants du produit (voir "Mises en garde et précautions").
Même si un premier traitement par TISSEEL a été bien toléré, une administration ultérieure du produit ou une administration systémique d'aprotinine peut entraîner des réactions anaphylactiques graves.
Les composants de la colle de fibrine provoquent rarement la formation d'anticorps.
Une injection intravasculaire peut entraîner des événements thromboemboliques, ainsi qu'un risque de réactions anaphylactiques.
TISSEEL devrait être utilisé avec prudence spécialement lors d'opérations de pontage coronarien, afin de minimiser tout risque d'utilisation intravasculaire.
Pour d'informations concernant la sécurité virale, voir "Mises en garde et précautions".
Lors d'études cliniques et pendant la surveillance post-marketing (marquée d'un p dans la liste ci-dessous) avec les colles de fibrine Baxter, les effets indésirables suivants avec TISSEEL ont été rapportés.
Dans les études cliniques, TISSEEL a été administré comme hémostatique supplémentaire lors d'interventions de chirurgie cardiaque, vasculaire, prothétique de hanche, du foie et de la rate. Autres études cliniques ont inclus le collage de vaisseaux lymphatiques chez des patients subissant un curage ganglionnaire axillaire, le collage du anastomoses coliques et collage de la dura dans la fosse postérieure. Comme la fréquence des effets indésirables rapportés pendant la surveillance post-marketing ne peut pas être estimée sur la base des données disponibles, la limite supérieure de l'intervalle de confiance à 95% a été, chaque fois que possible, calculée comme suit, en utilisant la règle de trois: 3/1146 = 0,0026 ou 0,26% c.-à-d. occasionnels («1146» étant le nombre total de patients traités dans des études cliniques réalisées avec TISSEEL).
Très fréquent (≥1/10), fréquent (≥1/100 à <1/10), peu fréquent (≥1/1,000 à <1/100), rare (≥1/10,000 à <1/1,000), très rare (<1/10,000), fréquence inconnue (ne peut être estimée sur la base des données disponibles).
Domaines généraux | Effets indésirables | Fréquence |
Infections et infestations | Infection post-opératoire des plaies | fréquents |
Affections hématologiques et du système lymphatique | Augmentation des produits de dégradation de la fibrine | occasionnels |
Troubles du système immunitaire | Réactions d'hypersensibilité* p | occasionnels |
Réactions anaphylactiques* p | occasionnels | |
Choc anaphylactique* p | occasionnels | |
Paresthésie p | occasionnels | |
Bronchospasme p | occasionnels | |
Sibilances p | occasionnels | |
Prurit p | occasionnels | |
Erythème p | occasionnels | |
Troubles du système nerveux | Dysesthésies | fréquents |
Troubles fonctionnels cardiaques | Bradycardie p | occasionnels |
Tachycardie p | occasionnels | |
Troubles fonctionnels vasculaires | Thrombose veineuse axillaire ** | fréquents |
Hypotension | rares | |
Hématomes p | occasionnels | |
Embolie artérielle p | occasionnels | |
Embolie pulmonaire *** p | inconnue | |
Embolie artérielle cérébrale p | occasionnels | |
Infarctus cérébral** p | occasionnels | |
Troubles fonctionnels respiratoires, thoraciques et médiastinaux | Dyspnée p | occasionnels |
Troubles gastro-intestinaux | Nausées | occasionnels |
Occlusion intestinale p | occasionnels | |
Troubles fonctionnels de la peau et du tissu sous-cutané | Éruption cutanée | fréquents |
Urticaire p | occasionnels | |
Retard de cicatrisation d'une plaie p | occasionnels | |
Affections musculosquelettiques et systémiques | Douleurs des membres | fréquents |
Troubles généraux et réactions au site d'application | Douleurs | fréquents |
Hausse de la température corporelle | fréquents | |
Rougeur cutanée p | occasionnels | |
Œdèmes p | occasionnels | |
Blessures et intoxications | Douleurs post-procédurales | occasionnels |
Sérome | très fréquent | |
Angiooedème p | occasionnels |
* les réactions anaphylactiques et le choc anaphylactique incluent des réactions fatales.
** comme conséquence d'une application intravasculaire dans le sinus pétreux supérieur.
*** comme avec d'autres colles de fibrine, des embolies aériennes et gazeuses potentiellement mortelles/mortelles sont survenues sous TISSEEL lors de l'utilisation de gaz comprimé. Ces événements semblent être liés à l'utilisation incorrecte d'un dispositif d'application par pulvérisation (p.ex. pression plus élevée que celle recommandée et à une distance trop proche des tissus).
p effets indésirables observés pendant la surveillance post-marketing
Effets de classe
Les autres effets indésirables associés à des colles de fibrine/hémostatiques incluent des réactions d'hypersensibilité pouvant se manifester par une irritation au site d'application, des symptômes thoraciques, des frissons, des céphalées, une léthargie, une agitation et des vomissements.
Surdosage
La colle de fibrine ne doit être appliquée qu'en couche mince car des couches trop épaisses peuvent perturber l'efficacité de la préparation et le processus de cicatrisation.
Propriétés/Effets
Code ATC: B02BC30
La colle de fibrine TISSEEL est une colle biologique à deux composants. Les deux composants sont congelés et doivent être décongelés avant l'emploi. Les deux composants (la solution de colle de protéine et la solution de thrombine) sont mélangés pendant ou immédiatement avant l'utilisation (voir méthode d'application). Il se forme une solution visqueuse de colle de protéine-thrombine qui se transforme rapidement en une masse blanche élastique, adhérant fortement au tissu. Cette solidification qui se déroule d'une manière analogue au processus physiologique de la coagulation, assure l'hémostase, la fermeture des plaies et le collage de tissus. La colle de fibrine solidifiée est entièrement résorbée au cours de la cicatrisation.
Le schéma suivant a pour but d'expliquer le déroulement:
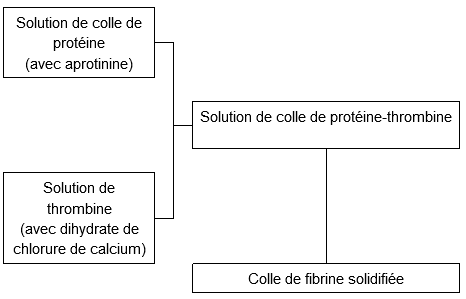
Pharmacocinétique
D'une manière analogue au dernier stade de la coagulation sanguine physiologique, le collage par la fibrine conduit en l'espace de quelques minutes à la formation d'une trame de fibrine physiologique. Cette trame qui a la forme d'un réseau tridimensionnel, est ensuite colonisée par des fibroblastes. La mise en route de la synthèse de collagène par les fibroblastes conduit à une organisation conjonctive de la zone lésionnelle.
En même temps se produit une résorption progressive de la fibrine, l'examen histomorphologique ne montrant aucune différence avec la dégradation de la fibrine extravasculaire autologue. La vitesse de dégradation de la fibrine est influencée d'une part par l'activité fibrinolytique des tissus voisins et par l'afflux de granulocytes et d'autre part par la quantité d'aprotinine, un antifibrinolytique, additionnée à la colle. Sous l'effet d'activateurs du plasminogène du tissu environnant, la faible quantité de plasminogène contenue dans TISSEEL est transformée en plasmine qui dégrade la fibrine en produits de dégradation solubles (PDF). Les produits de dégradation de la fibrine sont phagocytés, puis encore plus dégradés, par les granulocytes et les macrophages qui ont, avec les fibroblastes, envahi la zone lésionnelle.
La thrombine forme un complexe avec l'antithrombine III. Ce complexe et l'aprotinine sont dégradés par protéolyse, tandis que le CaCl2 se retrouve dans le bilan électrolytique.
Les profils pharmacocinétiques ont permis de mettre en évidence la bioéquivalence de l'aprotinine d'origine bovine et de l'aprotinine d'origine synthétique.
Données précliniques
TISSEEL avec aprotinine (d'origine bovine ou synthétique) a été bien toléré lors des études in vivo et des études de cicatrisation de ce type menées chez le rat et le lapin.
Dans les cultures de fibroblastes humains, la solution de colle de protéine de TISSEEL a montré une compatibilité cellulaire et aucune cytotoxicité. En outre, des tests in vitro appropriés n'ont pas révélé d'effets mutagènes.
Des études de toxicité sous-cutanée aiguë chez le rat et le lapin n'ont pas démontré de toxicité aiguë de TISSEEL et ont révélé une bonne tolérance locale. L'aprotinine d'origine bovine et l'aprotinine d'origine synthétique ont été tolérées même après application intraveineuse ou paraveineuse unique à très fortes doses (jusqu'à 1 500 000 IU/kg) chez le rat ou la souris. Les no-observed adverse event effect level ont été définies <100 000 IU/kg (souris) et <200 000 IU/kg (rat). Des modèles appropriés de cochons d'Inde n'ont montré ni signe de potentiel anaphylactique, ni signe de potentiel sensibilisant de l'aprotinine d'origine bovine ou synthétique.
Une analyse systématique de la littérature a également permis d'exclure des effets indésirables ou une toxicité des solvants / détergents / réactifs utilisés pour TISSEEL.
Remarques particulières
Incompatibilités
Des produits contenant de la cellulose oxydée peuvent réduire l'efficacité de TISSEEL. Pour cette raison ces produits ne devraient pas être utilisés comme matériau porteur.
TISSEEL ne peut pas être mélangé avec d'autres médicaments.
A cause de la dénaturation des protéines ou d'autres mécanismes des solutions contenant de l'alcool, de l'iode ou des métaux lourds interfères avec l'efficacité du produit. Si leur emploi s'avère inévitable, éliminer le plus complètement possible tout éventuel résidu avant de commencer le collage.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Utiliser les solutions décongelées dans un délai maximum de 72 heures après la décongélation. Jusqu'à l'emploi, conserver à température ambiante (15 – 25 °C) dans l'emballage stérile non ouvert et non endommagé.
Ne plus congeler et ne pas conserver au réfrigérateur après la décongélation !
Remarques concernant le stockage
Conserver congelé (≤-20 °C). Ne pas interrompre la chaîne du froid jusqu'à l'emploi.
Conserver dans l'emballage original, à l'abri de la lumière. Tenir hors de la portée des enfants !
Remarques concernant la manipulation
Généralités
Avant d'appliquer TISSEEL, couvrir soigneusement toutes les parties du corps non concernées par l'application, pour éviter une adhésion tissulaire sur des sites non souhaités.
Humidifier les gants et les instruments pouvant entrer en contact avec la solution de colle de protéine-thrombine avec une solution de chlorure de sodium stérile pour éviter une adhérence de la colle de fibrine. Une application séparée, séquentielle des deux composants doit être évitée.
Cela signifie que les deux composants doivent être appliqués ensemble et ne peuvent pas être appliqués séparément.
Manipulation et préparation
Les solutions de colle de protéine et de thrombine sont contenues dans une seringue pré-remplie à usage unique. Le produit est emballé aseptiquement dans deux sachets stérilisés. Le sachet interne est stérile tant que l'intégrité du sachet externe n'est pas rompue.
Il est recommandé de décongeler puis de réchauffer les deux composés au bain-marie d'eau stérile à une température de 33-37 °C. La température du bain ne doit pas dépasser 37 °C. (La température doit être contrôlée à l'aide d'un thermomètre et l'eau renouvelée si nécessaire. Il faut sortir la seringue pré-remplie de ses sachets avant de la plonger dans le bain-marie d'eau pour décongélation et réchauffement).
Le capuchon de la seringue ne doit pas être enlevé tant que la décongélation n'est pas terminée et que l'embout d'application n'est pas prêt à être connecté. Ne pas utiliser TISSEEL tant qu'il n'est pas complètement décongelé.
La décongelation et le réchauffement de la seringue préremplie peuvent être réalisés selon une des quatre modalités suivantes:
1. Décongélation / réchauffement rapide (bain-marie d'eau stérile) – méthode recommandée
Transférer le sachet intérieur dans le champ stérile, retirer la seringue pré-remplie du sachet intérieur et la placer directement dans le bain-marie stérile. Vérifier que le contenu de la seringue pré-remplie est entièrement immergé dans l'eau.
Tableau 1: Durées de décongélation et de réchauffement avec un bain-marie d'eau stérile à une température de 33 à 37 °C maximum.
Présentation | Durée minimale de décongélation et de réchauffement à 33 °C jusqu'à 37 °C maximum dans un bain-marie d'eau stérile |
Seringue PRIMA | |
2 ml | 5 minutes |
4 ml | 5 minutes |
2. Décongélation / réchauffement à l'aide d'un bain-marie non stérile
Alternativement, le produit peut être décongelé hors du champ stérile à l'aide d'un bain-marie non stérile.
Laisser la seringue pré-remplie dans les deux sachets et placer l'ensemble dans un bain-marie hors du champ stérile pendant la durée appropriée (voir tableau 2). Vérifier que les sachets restent immergés pendant toute la décongélation. Retirer du bain-marie après décongélation, sécher le sachet extérieur et transférer le sachet intérieur contenant la seringue pré-remplie et le piston dans le champ stérile.
Tableau 2: durées de décongélation et de réchauffement hors du champ stérile avec bain-marie non stérile à une température de 33 à 37 °C maximum.
Présentation | Durée minimale de décongélation et de réchauffement à 33 °C jusqu'à 37 °C maximum dans un bain-marie d'eau non stérile (Produit dans ses sachets) |
Seringue PRIMA | |
2 ml | 15 minutes |
4 ml | 20 minutes |
3. Décongélation et réchauffement dans un incubateur
Alternativement, les composants de la colle peuvent également être décongelées et réchauffées dans un incubateur entre 33 °C et 37 °C.
Les durées de décongélation et de réchauffement dans un incubateur sont reportées dans le tableau 3 ci-dessous. Les durées sont données pour le produit conservé dans ses sachets.
Tableau 3: Durées de décongélation et de réchauffement dans un incubateur entre 33 °C et 37 °C maximum.
Présentation | Durée minimale de décongélation et de réchauffement à 33 °C jusqu'à 37 °C maximum dans un incubateur (Produit dans ses sachets) |
Seringue PRIMA | |
2 ml | 40 minutes |
4 ml | 50 minutes |
4. Décongélation à température ambiante (ne dépassant pas 25 °C) / Réchauffement avant l'utilisation dans un incubateur de 33 °C à 37 °C
Le produit peut être décongelé à température ambiante. Les durées fournies dans le tableau 4 sont les durées minimums nécessaires pour une décongélation à température ambiante. Après décongélation, la préparation doit être conservée à la température ambiante et utilisée dans les 72 heures. Lorsque le produit a été décongelé à température ambiante, il doit ensuite être réchauffé entre 33 °C et 37 °C dans un incubateur avant l'utilisation. Les durées de décongélation correspondantes sont indiquées dans le tableau 4.
Tableau 4: Durées de décongélation à température ambiante suivies d'un réchauffement dans un incubateur entre 33 °C et 37 °C maximum, avant utilisation
Présentation | Durée minimale de la décongélation à température ambiante (ne dépassant pas 25 °C), suivie d'un réchauffement supplémentaire avant l'utilisation dans un incubateur à 33 °C jusqu'à 37 °C maximum (Produit dans ses sachets) | |
Seringue PRIMA | ||
Durée de décongélation à température ambiante | Durée de réchauffement dans un incubateur | |
2 ml | 80 minutes | + 11 minutes |
4 ml | 90 minutes | + 13 minutes |
Ne pas décongeler le produit dans ses mains !
Ne pas réchauffer à la micro-onde !
Après décongélation, ne pas remettre au réfrigérateur ni au congélateur !
Les sachets décongelés à température ambiante, non ouvertes, peuvent être stockés pendant 72 heures maximum à température ambiante contrôlée (ne dépassant pas +25 °C). Si le produit n'a pas été utilisé dans les 72 heures suivant la décongélation, il doit être éliminé.
Pour assurer un mélange optimal des deux solutions, les deux composants doivent être réchauffés à une température de 33 à 37 °C immédiatement avant utilisation. TISSEEL ne doit pas être exposé à des températures dépassant 37 °C et ne doit pas être mis dans la micro-onde. La solution protéinique et la solution de thrombine doivent être limpides ou légèrement opalescentes. Ne pas utiliser de solutions troubles ou présentant des dépôts. Les produits décongelés doivent être inspectés visuellement afin de vérifier l'absence de particules et de coloration anormale avant administration.
La solution protéinique, une fois décongelée, doit être un liquide légèrement visqueux. Si elle a la consistance d'un gel solidifié, elle doit être considérée comme dénaturée (par exemple, en raison d'une interruption de la chaîne du froid ou par un surchauffage pendant le réchauffement). Dans ce cas, TISSEEL ne doit pas être utilisé.
Retirer la seringue du sachet juste avant l'emploi. Les capuchons de protection des seringues ne doivent pas être retirés des seringues qu'avant l'emploi.
Déplacer d'abord le capuchon d'avant en arrière pour pouvoir retirer plus facilement le capuchon de protection de la seringue PRIMA. Ne retirer le capuchon de protection qu'après cette procédure.
Ne commencer à utiliser TISSEEL que lorsque la préparation est entièrement décongelée et a atteint de 33 à 37 °C (consistance fluide).
Pour plus d'informations relatives à la préparation, veuillez-vous adresser à l'infirmière ou au médecin responsable.
Administration avec la seringue PRIMA
Pour l'application, la seringue à double chambre avec les solutions de protéines adhésives et de thrombine doit être connectée à une pièce de raccordement et à une canule d'application, fournies dans le set de dispositifs d'application.
Le double piston pour la seringue à double chambre permet de délivrer des volumes identiques au travers de la pièce de raccordement avant d'être mélangés dans la canule d'application puis appliqués.
Instructions d'utilisation de la seringue PRIMA
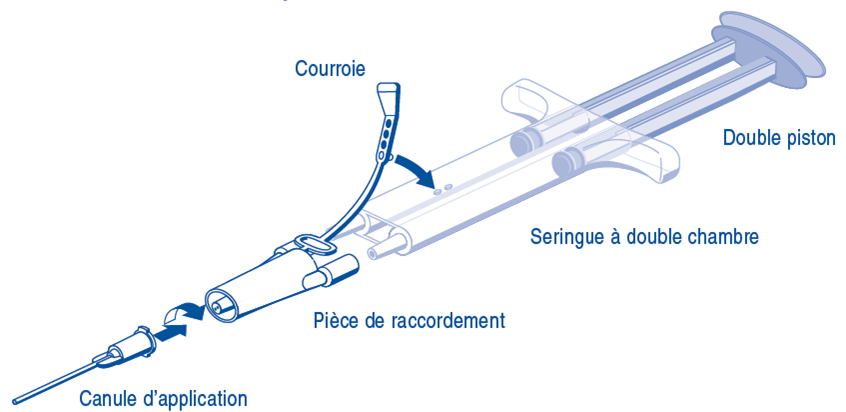
1.Expulser tout l'air de la seringue avant de fixer tout dispositif d'application.
2.Aligner la pièce de raccordement et l'attache sur le côté de la seringue avec le trou de la sangle d'attache.
3.Connecter les embouts de la seringue à double chambre à la pièce de raccordement en veillant à ce qu'ils soient fixés fermement. S'assurer de leur bon emboîtement.
Attacher la pièce de raccordement à la seringue à double chambre à l'aide de l'attache de sécurité.
Si l'attache de sécurité se déchire, utiliser la pièce de raccordement de secours.
Si aucune pièce de raccordement n'est plus disponible, on peut toujours utiliser la seringue, mais il faut surveiller la pièce de raccordement et veiller à ce qu'elle reste bien attachée pour prévenir le risque de fuites.
Ne pas expulser l'air présent dans la pièce de raccordement.
4.Fixer une canule d'application sur la pièce de raccordement. Ne purger l'air restant dans la pièce de raccordement ou dans la canule d'application qu'au dernier moment, juste avant l'application, sinon l'orifice de la canule risque de s'obstruer.
Remarque:
Avant d'appliquer TISSEEL, la surface de la plaie doit être séchée à l'aide des techniques classiques (p.ex. l'application intermittente de compresses ou de tampons, utilisation de dispositifs d'aspiration). Ne pas utiliser d'air comprimé ni de gaz pour sécher le site d'application.
Appliquer le mélange de solution de protéines pour colle et de de solution de thrombine sur la surface d'application ou sur la surface des parties à coller en appuyant lentement sur l'arrière du double piston.
Dans les interventions chirurgicales nécessitant l'utilisation de volumes minimaux de colle de fibrine, il est recommandé d'expulser et de jeter les premières gouttes de produit.
Après l'application de TISSEEL, attendre au moins 2 minutes pour permettre une polymérisation suffisante.
Si l'application des composants de la colle de fibrine est interrompue, il est possible que la canule soit obstruée par coagulation. Remplacer la canule d'application par une nouvelle canule juste avant la reprise de l'application. Si les ouvertures de la pièce de raccordement sont obstruées, utiliser la pièce de raccordement de rechange fournie avec le kit.
Remarque : En raison de la forte concentration de la solution de thrombine (500 U.I./ml), la prise de la colle de fibrine commence déjà quelques secondes après le mélange des composants.
L'application est également possible avec d'autres accessoires fournis par BAXTER spécialement adaptés, par exemple, a une intervention sous endoscopie, à la chirurgie peu invasive ou à l'application sur de grandes surfaces ou des zones difficiles d'accès. Lors de l'utilisation de ces dispositifs d'application, respecter scrupuleusement les instructions d'utilisation correspondantes.
Après l'application attendre au moins 2 minutes afin d'obtenir une polymérisation suffisante.
TISSEEL est parfois utilisée aussi en association avec des matériaux biocompatibles, par exemple les compresses de collagène qui servent de soutien et de renforcement.
Lors de l'application de TISSEEL à l'aide d'un dispositif de pulvérisation, veiller à utiliser une pression et une distance avec le tissu conformes aux limites recommandées par le fabricant comme suit:
Recommandations concernant la pression, la distance et les dispositifs pour l'application par pulvérisation de TISSEEL | |||||
Chirurgie | Dispositif de pulvérisation à utiliser | Embouts applicateurs à utiliser | Dispositif de contrôle de la pression à utiliser | Distance recommandée avec le tissu cible | Pression de pulvérisation recommandée |
Plaie ouverte | Tisseel / Artiss Spray Set | S.O. | EasySpray | 10-15 cm | 1,5-2,0 bars |
Tisseel / Artiss Spray Set - boîte de 10 | S.O. | EasySpray | |||
Procédures laparoscopiques/peu invasives | S.O. | Duplospray MIS Applicator 20 cm | Duplospray MIS Regulator | 2 – 5 cm | 1,2-1,5 bar (18-22 psi) |
Duplospray MIS Regulator NIST B11 | |||||
Duplospray MIS Applicator 30 cm | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Duplospray MIS Applicator 40 cm | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Embout amovible | Duplospray MIS Regulator | ||||
Duplospray MIS Regulator NIST B11 | |||||
Lors de la pulvérisation de TISSEEL, il convient de surveiller tout changement de pression artérielle, de fréquence cardiaque, de saturation en oxygène et de CO2 de fin d'expiration en raison du risque d'embolie gazeuse (voir également "Posologie/Mode d'emploi" et "Mises en garde et précautions".
Numéro d’autorisation
52'618 (Swissmedic)
Titulaire de l’autorisation
Baxter AG, 8152 Opfikon
Mise à jour de l’information
Janvier 2018
Reviews (0)
Recently Viewed

Free consultation with an experienced pharmacist
Describe the symptoms or the right drug - we will help you choose its dosage or analogue, place an order with home delivery or just consult.
We are 14 pharmacists and 0 bots. We will always be in touch with you and will be able to communicate at any time.

 Deutsch
Deutsch French
French